|
|
登陆查看更多优秀资源帖,与同道便捷交流讨论
您需要 登录 才可以下载或查看,没有帐号?立即注册
x
来源:中华病理学杂志
作者:崔秀杰,张春燕,张晓芳,王妍,刘志艳(山东大学齐鲁医院病理科;山东大学基础医学院病理学系)苏鹏(山东大学齐鲁医院病理科)吕斌(山东大学齐鲁医院普外科)任玉波(山东省聊城市人民医院病理科)樊祥山(江苏省南京市鼓楼医院病理科)宋云河(山东大学临床医学院)
本文经《中华病理学杂志》授权发布,其他媒体转载或引用须经《中华病理学杂志》同意,否则追究法律责任。
【摘要】目的:探讨头颈部显示胸腺样分化的癌(carcinoma showing thymus like elements,CASTLE)的细胞学特点及临床病理特征。方法:收集7例CASTLE患者存档资料,行细胞学、组织学观察及免疫组织化学(LASB法)染色,采用突变扩增阻滞系统(ARMS)法检测BRAFV600E基因突变,并采用EBER原位杂交检测EB病毒感染情况,分析其细胞学特点及临床病理特征。结果:7例患者,5例女性,2例男性。年龄49~78岁,平均年龄65.6岁。6例位于甲状腺内,1例位于下咽。7例均为孤立性结节,边界相对清楚。肿瘤直径1.7~4.1cm,平均直径3.0cm。4例(含下咽病例)伴有颈部淋巴结转移。7例均有随访。1例于甲状腺内原位复发,并行甲状腺细针穿刺。其余6例均未发现复发和转移。1例CASTLE局灶性表达CD5(小于5%肿瘤细胞),30%肿瘤细胞表达突触素,其余6例CASTLE弥漫阳性表达CD5。所有病例阳性表达CK5/6、p63、CD117,不表达甲状腺转录因子1、甲状腺球蛋白、CT。Ki-67阳性指数在3%~90%。6例均无BRAFV600E基因突变。6例EBER原位杂交均为阴性。结论:位于下咽CASTLE具有和甲状腺内CASTLE相同形态学特点和免疫组织化学表型。CD5和CD117是诊断CASTLE的有效指标。CD5阴性的CASTLE可伴神经内分泌分化。CASTLE的Ki-67阳性指数可以较高,在淋巴上皮癌型CASTLE中尤为明显。BRAFV600E基因突变和EB病毒感染可能不参与CASTLE的发生。
显示胸腺样分化的癌(carcinoma showing thymus like element, CASTLE)是发生于头颈部的一种罕见肿瘤,主要见于甲状腺内,少数可位于甲状腺外邻近软组织[1]。由于其发生率较低,对其生物学行为了解有限,但多数CASTLE的预后较好。甲状腺外CASTLE目前全球仅有3例报道[2],国内尚未检索出这方面资料,因而对其临床病理特征鲜有报道。由于本病临床病史缺乏特异性,术前难以诊断;病理组织学检查时也极易与鳞状细胞癌、低分化癌及未分化癌等预后差的肿瘤相混淆而造成过诊、误诊。我们回顾性分析研究了7例头颈部CASTLE,总结其临床病理特征,以期加强对本病的认识。
资料与方法
1.病例资料:
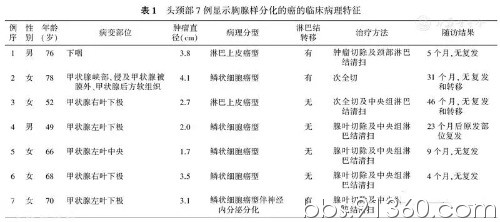
收集2011年1月至2016年9月山东大学齐鲁医院常规及会诊、南京鼓楼医院会诊为CASTLE的病例共7例,收集患者的临床病理信息,并对患者进行随访(表1)。
2.方法:
所有标本均经3.7%中性甲醛液室温固定,石蜡包埋,5μm厚常规切片及HE染色。由两位高年资病理医师,参照2014年美国部队病理研究院(Armed Forces Institute of Pathology,AFIP)《甲状腺和甲状旁腺肿瘤》中CASTLE诊断标准,行形态学观察(双盲)。免疫组织化学采用LSAB法,一抗包括CK5/6、p63、CD5、甲状腺转录因子(TTF)1、甲状腺球蛋白(TG)、降钙素、嗜铬粒素A(CgA)、突触素、CD117、Ki-67。采用突变扩增阻滞系统(ARMS)法检测BRAFV600E基因突变。采用EBER原位杂交检测EB病毒感染情况。一抗试剂盒购自北京中杉金桥生物技术有限公司。免疫组织化学染色和原位杂交均设阴性对照和阳性对照。
结果
1.临床特征:
7例患者,男性2例,女性5例,年龄49~78岁,平均年龄65.6岁。肿瘤部位:6例位于甲状腺内,左叶多于右叶,1例位于下咽梨状窝。6例患者以颈部结节为主诉,1例为常规体检检出。2例主诉有颈部压迫症状。下咽病例有吞咽异物感2个月余。实验室检查:TG、促甲状腺素(TSH)、T3、T4、甲状腺过氧化物酶(TPO)水平正常。影像学表现:7例均为单发肿块(图1),3例提示边界不清。患者行肿瘤切除、次全切、腺叶切除和/或中央组淋巴结清扫。所有病例均未行放疗及化学疗法。均获得随访,仅1例术后23个月原发部位复发而行甲状腺细针穿刺细胞学检查,随访期间无死亡病例(表1)。
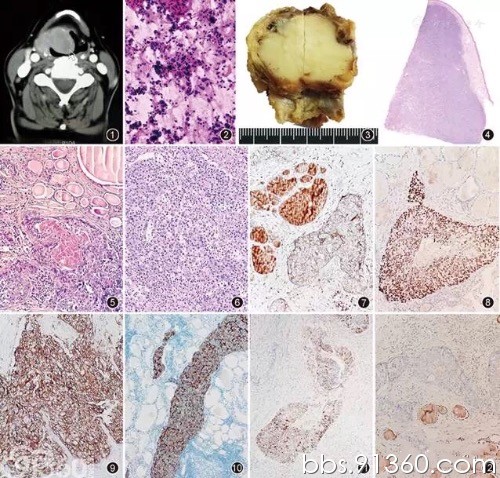
图1 CT检查,下咽见一低回声结节性病灶,大部分边界相对清楚,局灶边界不清(箭头)
图2 头颈部显示胸腺部分化的癌,淋巴细胞背景中散在肿瘤细胞团,缺乏乳头状和滤泡结构,细胞大小不一,圆形、椭圆形或小的裸核短梭形细胞;核仁明显,部分细胞质内呈空泡状 HE 高倍放大
图3 肿瘤与周围软组织界限相对清楚,呈推挤性边界,质地较实,直径约3.8cm,切面象牙白色,无出血、坏死、囊性变及钙化
图4 肿瘤位于皮下,缺乏包膜,呈膨胀性生长,界限相对清楚 HE 低倍放大
图5 鳞状细胞癌型CASTLE,肿瘤细胞呈大小不等的巢状或交互吻合的梁带状结构,局部侵袭周围甲状腺组织,可出现不同程度的角化和鳞状分化 LSAB法 高倍放大
图6 淋巴上皮癌型CASTLE:肿瘤细胞巢之间有或缺乏宽大的纤维间隔,分叶状结构较明显,间质见较多淋巴细胞浸润,肿瘤细胞巢内也可见淋巴细胞浸润,肿瘤细胞圆形或者椭圆形,略嗜碱性,核仁明显
图7 CD5呈线状阳性表达于肿瘤细胞的细胞膜,并可见于少数淋巴细胞,但甲状腺滤泡上皮细胞无表达 LSAB法 高倍放大
图8 p63弥漫阳性表达于肿瘤细胞核,但甲状腺滤泡上皮细胞无表达 LSAB法 高倍放大
图9 CK5/6在所有病例中均弥漫强阳性表达于肿瘤细胞质 LSAB法 高倍放大
图10 CD117在所有肿瘤中均呈不同程度阳性表达于肿瘤细胞质(例7) LSAB法 中倍放大
图11 突触素阳性表达于肿瘤细胞质(例7) LSAB法 中倍放大
图12 肿瘤细胞均不表达甲状腺转录因子1,而内对照甲状腺滤泡上皮细胞呈阳性表达 LSAB法 中倍放大
2.病理特点:
(1)穿刺细胞学特点:例4复发肿瘤甲状腺细针穿刺显示典型CASTLE细胞学特点。镜下可见淋巴细胞背景中散在肿瘤细胞团,缺乏乳头状结构和滤泡结构,细胞大小不一,圆形、椭圆形或小的裸核短梭形细胞;核仁明显,部分细胞质内呈空泡状;可见个别细胞呈鳞状分化(图2)。(2)大体检查:均无包膜,界限相对清楚,呈推挤性边界;质地较实(图3)。肿瘤直径1.7~4.1cm,平均直径3.0cm。切面呈分叶状,甲醛固定后呈象牙白色,无出血、坏死及钙化。肿瘤与周围组织之间界限清楚。(3)组织学检查:低倍镜下,肿瘤缺乏包膜,呈膨胀性生长(图4)。肿瘤细胞呈大小不等的巢状或交互吻合的梁带状结构,局部侵袭周围组织,可出现不同程度的角化和鳞状分化(图5)。肿瘤分叶状结构较明显,间质和肿瘤细胞巢内均可见较多淋巴细胞浸润。高倍镜下,癌细胞呈多角形或短梭形,细胞间界限不十分清楚,多呈合体状,常呈弱嗜酸性。核呈较大卵圆形、泡状,其内可见清晰的小核仁,核分裂象约(1~3)/10HPF(图6)。(4)免疫组织化学染色:CD5呈不同程度线状阳性表达于肿瘤细胞的细胞膜及少数淋巴细胞(图7)、p63弥漫阳性表达于肿瘤细胞核(图8)、CK5/6在所有病例中均为细胞质弥漫强阳性(图9);CD117呈不同程度阳性表达于肿瘤细胞质(图10)。仅1例突触素阳性表达于30%肿瘤细胞中(图11)。肿瘤细胞均不表达TTF1(图12)、TG和降钙素。Ki-67阳性指数在3%~90%之间。(5)分子检测:EBER原位杂交:阴性。BRAFV600E均为野生型。
讨论
Miyauchi等[3]最早于1985年报道了3例甲状腺内上皮性胸腺瘤(intrathyroidal epithelial thymoma,ITET)。1988年Kakudo等[4]指出其可能来源于异位的胸腺组织。同年,Asa等[5]指出,起源于异位胸腺组织的病变是一组独立病变。1989年Rosai[6]将其视为独立病种,1991年Chan和Rosai[7]报道了11例并更名为CASTLE,并将甲状腺内伴有胸腺分化的肿瘤分为3型,其中异位胸腺瘤为CASTLE对应的良性形式。2004年第3版WHO肿瘤内分泌分册将CASTLE作为甲状腺独立的肿瘤分类,并指出其为低度恶性肿瘤。
迄今报道100余例CASTLE,多见于亚洲国家,发病率约0.083%[8]。头颈部甲状腺外CASTLE仅有3例报道[2],本组下咽病例为全球第4例。患者平均年龄为65.6岁,女性多于男性,均略高于前期报道[9]。Kakudo等[8]将CASTLE分为3种亚型,包括鳞状细胞癌型、淋巴上皮癌型或基底细胞样型、神经内分泌癌型,本组病例为前2型,以鳞状细胞癌型为主,提示鳞状细胞癌型较为多见,尤应警惕其与原发鳞状细胞癌的鉴别。神经内分泌癌型较为少见。
CD5、CD117被认为是诊断CASTLE较为特异的免疫组织化学指标,但也有罕见CD5阴性CASTLE的报道。本组病例肿瘤细胞呈巢状结构,伴有或不伴有粉刺样坏死,但肿瘤呈浸润性生长,可鉴别异位胸腺瘤。肿瘤与周围甲状腺组织境界相对清楚,缺乏病理性核分裂象,可鉴别甲状腺低分化癌和未分化癌。CD5和CD117阳性,有助于与原发鳞状细胞癌鉴别。例7少于5%的肿瘤细胞表达CD5,但大部分表达CD117,支持CD5阴性的CASTLE的诊断。同时,该病例伴有粉刺样坏死,但Ki-67阳性指数仅为3%,提示CASTLE内粉刺样坏死与肿瘤细胞增殖活性之间不存在必然联系。该病例还提示,对于CD5阴性的病例,应加做CD117,以除外CD5阴性CASTLE的可能。该肿瘤约30%肿瘤细胞表达突触素,但不表达CgA,提示肿瘤伴有神经内分泌分化。降钙素、TG和TTF1阴性表达,可除外甲状腺髓样癌及乳头状癌、滤泡癌。但CASTLE病例CD5失表达过程中是否必然伴神经内分泌分化,尚需更多病例验证。
Ki-67阳性指数为3%~90%,其中淋巴上皮癌型偏高于鳞状细胞癌型。下咽病例Ki-67阳性指数高达90%,为目前已有报道中最高的病例,尚需进一步随访。6个病例EBER原位杂交结果均为阴性,支持EB病毒不参与CASTLE发生的推论[8,10]。
例4为术后复发会诊病例。原单位术中快速及术后病理诊断“甲状腺低分化癌”,提示CASTLE易误诊为低分化癌。患者复发肿瘤细胞涂片显示细胞密集,细胞中度异型,提示恶性肿瘤;不伴有乳头结构和滤泡结构的大的细胞团,可鉴别甲状腺乳头状癌和滤泡癌;核仁明显、不具有“椒盐核”特点,可鉴别甲状腺髓样癌;尽管少数角化细胞的出现,提示鳞状细胞癌可能,但细胞质内空泡(intracytoplasmic lumina)提示CASTLE可能。遂会诊原单位首次手术切片并行免疫组织化学染色,CD5、CK5/6、p63、CD117均阳性表达,其余标志物均阴性表达,诊断为CASTLE,鳞状细胞癌型。本例提示,CASTLE具有独特的细胞学特点,在甲状腺细针穿刺诊断中应提高警惕,注意鉴别诊断,必要时可对细胞学标本行免疫组织化学染色CD5、CD117以辅助诊断。
CASTLE的5年生存率和10年生存率分别为90%和82%[11],发现时可伴有区域性淋巴结转移,晚期可伴有血道转移,但死亡病例少见[4]。本组病例所有患者均采取手术治疗,术后未行放化疗、仅行TSH抑制治疗。4个病例伴有同侧颈部淋巴结转移,其中1例术后复发,提示淋巴结转移与肿瘤复发有关。但所有患者随访期间均无远处转移,无生命危险,提示CASTLE预后好于低分化癌和鳞状细胞癌。
综上所述,头颈部甲状腺外CASTLE具有和甲状腺内CASTLE相同的临床病理学特点。因其预后好于鳞状细胞癌和低分化癌,当引起重视、避免误诊、过诊。尤其甲状腺外CASTLE,因罕见及具有良好的生物学行为,其病理诊断尤应引起重视。CD5阴性的CASTLE可伴有神经内分泌分化,提示CD5阴性病例应加做CD117等以明确诊断。BRAFV600E基因突变和EB病毒感染并非CASTLE发生的原因。 |
-
-
|