登陆查看更多优秀资源帖,与同道便捷交流讨论
您需要 登录 才可以下载或查看,没有帐号?立即注册
x
人体每天都会产生上亿个死亡细胞。将旧细胞清除,给新的细胞留出位置,才能够使组织或器官保持活力与稳态。如果清除过程不顺利,则有可能会导致不良后果,如系统性红斑狼疮诱因之一就是凋亡细胞的积累诱发细胞继发性坏死,释放与损伤相关的分子模式,导致大范围的炎症反应。因此,清除死亡细胞对维持体内平衡具有重要意义。 胞葬作用 (Efferocytosis) 就是指吞噬细胞清除程序性死亡细胞的过程。在大多数组织中,胞葬作用由专职性吞噬细胞 (巨噬细胞和树突细胞) 或垂死细胞附近的非专职性吞噬细胞 (上皮细胞和纤维细胞) 来完成。胞葬作用能够阻止垂死细胞发生继发性坏死,以免释放出可能引起炎症的有害细胞内容物 (如氧化物和蛋白酶)。那么吞噬细胞是如何识别垂死细胞并清除掉它们的呢?来听听胞葬作用的三部曲~Find-Eat-Digest~♪ 胞葬作用三部曲
垂死细胞会释放出可溶性介质,这些介质中就包含让吞噬细胞识别的“Find me” 信号,包括核苷酸 (如 ATP, UTP)、膜脂 (如磷酸鞘氨醇)、趋化因子 (如 CX3CL1) 等。这些信号不仅能吸引吞噬细胞,还能使吞噬细胞做好 “作战” 的准备,例如增强吞噬受体和消化机制的表达。 凋亡细胞的核苷酸 “Find me” 信号可通过 pannexin 通道 (被凋亡过程中 caspase 3/7的裂解激活) 释放 (图 1)。释放的 ATP 通过嘌呤受体 P2Y 诱导吞噬细胞迁移。此外,核苷酸还能够调节巨噬细胞的免疫机制。例如,凋亡细胞的 ATP 或 AMP 可转化为腺苷,腺苷再通过腺苷受体抑制炎症,上调抗炎 (anti-inflammatory) 和促消炎 (pro-resolution) 基因表达 (包括Nr4a1 和血小板反应蛋白)。 非凋亡细胞的脂膜完整性被破坏,炎症信号直接被释放到细胞外。被病原体感染的细胞会释放病原体相关分子模式 (PAMP),该信号可与吞噬细胞上或吞噬细胞中的模式识别受体 (PRR) 结合,影响巨噬细胞的功能和免疫激活。另外,非凋亡细胞也会释放损伤相关分子模式 (DAMP),触发炎症反应,可作为巨噬细胞的趋化因子。 图 1. 吞噬细胞识别凋亡细胞[1] 凋亡细胞释放“Find me” 信号 (核苷酸、膜脂、趋化因子等),吞噬细胞上相应的受体与之结合,诱导吞噬细胞迁移、上调抗炎/促消炎基因表达,以及调节细胞骨架 吞噬细胞迁移到凋亡细胞附近后,表面受体识别凋亡细胞的 “Eat me”信号,与之结合。“Eat me” 信号包括磷脂酰丝氨酸 (Phosphatidylserine, PS)、钙网蛋白、氧化低密度脂蛋白等,其中 PS 是最有效、进化上最保守的信号分子。所有形式的细胞死亡的一个共同特征是质膜中磷脂不对称性的丧失,PS就会暴露在细胞外,促进死亡细胞被吞噬。凋亡过程中,位于细胞内侧的 PS 会在早期阶段从内侧翻转到表面。吞噬细胞的 PS 受体可以直接或间接识别暴露在表面的 PS。BAI1 (PS 受体) 与 PS 结合后,通过 ELMO1-DOCK 复合物启动细胞内信号传导,以诱导 Rac1 介导的肌动蛋白细胞骨架重排 (图 2),为 “吃掉” 凋亡细胞做好准备。
与之相对的是,健康细胞表面暴露“Don't eat me” 信号,包括 CD47 和CD24。活细胞上的 CD47 与巨噬细胞的 SIRPα 结合,导致 SIRPα 胞质结构域的酪氨酸磷酸化,募集到的 SHP1/2 再通过非肌肉肌球蛋白 IIA 来抑制吞噬作用 (图 2)。这些信号能使健康细胞避免被吞噬细胞清除。 图2. 吞噬细胞结合凋亡细胞[1] 吞噬细胞直接 (BAI1, TIM1) 或间接 (AXL, MerTK) 识别凋亡细胞表面的 PS,激活 ELMO 和 DOC 蛋白的表达,进而激活 GTPase RAC1,增强肌动蛋白重塑和吞噬杯的形成。健康细胞表面的 CD47 能阻止被吞噬 在与垂死细胞结合后,吞噬细胞启动肌动蛋白重塑,质膜内陷及局部外溢形成吞噬体,通过胞吞作用将垂死细胞 “吃掉”。胞吞后形成吞噬体,吞噬体膜会发生多种生化变化,这些过程由 Rab GTPase 蛋白家族控制。吞噬体成熟后,通过形成 Ca2+依赖性 SNARE 复合物 (由VAMP7 和 Syntaxin 7 组成) 与溶酶体直接融合 (图 3a)。溶酶体内有大量蛋白酶、核酸酶和脂肪酶,可消化吞噬体中凋亡细胞。另外还有 LC3 (微管相关蛋白1A/1B-轻链 3) 相关吞噬作用 (LAP) 通路 (图 3b)。吞噬细胞吞噬垂死细胞后,LAPPI3K 复合物被募集到含有凋亡细胞的LAP相关吞噬体 (LAPosome),该复合物对 LAPosome 的保持至关重要,并且激活了 LC3 的连接机制。LC3 的连接促进了 LAPosome 与溶酶体融合,提高了清除死细胞的效率并且保持免疫沉默。 图 3. 吞噬细胞吞噬凋亡细胞[2] a. 溶酶体降解途径:VPS34 被募集到RAB5-positive早期吞噬体,催化磷脂酰肌醇形成 PI3P (这些都是吞噬体成熟所必需的物质),早期吞噬体成熟为晚期吞噬体后,最终与溶酶体融合。b. LAP 通路:LAP PI3K 复合物 (由 Beclin 1、VPS34、VPS15、UVRAG 和Rubicon 组成) 激活 LC3 与 LAPosome 的连接,促进 LAPosome 的成熟,以及与溶酶体融合
·垂死细胞的消化 溶酶体中含有大量蛋白酶、核酸酶、脂肪酶。吞噬体与溶酶体结合后,形成新的吞噬溶酶体 (Phagolysosome)。高酸度的环境 (pH=4.5~5.0) 和活性组织蛋白酶能降解垂死细胞。吞噬细胞还可重利用一些降解的垂死细胞成分。 大部分情况下,死亡细胞的数量都是远远超过吞噬细胞,所以吞噬细胞需要同时清除多个细胞。而垂死细胞带有膜、胆固醇、蛋白质、核酸等,这些物质需要被代谢。这对于吞噬细胞来说是巨大的负担,需要控制其自身的体积和表面积以及迅速改变免疫代谢环境。凋亡细胞本身也能改变吞噬细胞的免疫代谢 (图4):(1) 凋亡细胞表面的 PS 与受体结合后能激活或上调 LXR 和 ABCA1,可促进胆固醇的代谢与输出;(2) 凋亡细胞线粒体的脂肪酸氧化可促进抗炎因子 IL-10 的表达;(3) 吞噬细胞利用凋亡细胞的精氨酸 (Arginine) 驱动肌动蛋白细胞骨架重排,促进之后几轮的凋亡细胞摄取;(4) 糖酵解与葡萄糖输入的增加也促进 ATP 生成和肌动蛋白聚合。
图 4. 凋亡细胞调节吞噬细胞免疫代谢环境[1] 胞葬的动态追踪
常规的胞葬作用研究是在体外进行,例如使用原代人巨噬细胞和凋亡 Jurkat T 细胞进行免疫荧光染色后,可在显微镜下观察到胞葬作用的过程[3]。但由于凋亡细胞易被清除,在体内检测仍是个巨大的挑战。不过,办法总比困难多嘛~ Raymond 等人开发了一种基因编码的荧光报告基因 CharON,实现了在果蝇胚胎发育过程中胞葬作用的活细胞追踪[4]。这一研究结果于今年 3 月发表在 Science 杂志上。 研究者们首先设计了针对细胞凋亡和胞葬作用的传感器。针对细胞凋亡,他们设计了 一种绿色荧光蛋白 (GFP) 探针。细胞凋亡时表达的 caspases 3/7 能切割 GFP,使之发出荧光 (图 5a);GFP 在溶酶体的酸性条件下易淬灭,经突变 Q204H 基因后, GFP 对 pH 耐受。经过以上改造,他们设计出 pH 耐受的绿色荧光探针 pH-CaspGFP——它能准确地报告凋亡的细胞。针对吞噬作用,他们设计了一种新的红色荧光 pH 值传感器 pHlorina,它随着 pH 值的降低而增加荧光强度。最后将这两种传感器结合起来,获得探针 “CharON” (图 5b)。CharON 转基因的细胞,在凋亡时首先发绿色荧光,在被吞噬并在溶酶体内酸化后,随着 GFP 逐渐淬灭,pHlorina 的红色荧光强度增加。CharON 将连续性细胞事件可视化。 图 5. pH-CaspGFP 的设计 (a) CharON 探针检测胞葬过程 (b) 示意图[4] 细胞凋亡时,caspase 3/7 切割 GFP,发绿色荧光;被吞噬细胞吞噬后,在酸性环境中 GFP 逐渐淬灭,红色荧光 pHlorina 强度增加
为了追踪体内胞葬过程,研究者培育出CharON 转基因果蝇。在果蝇胚胎发育的中后期,发育中的中枢神经系统 (CNS) 有一波细胞凋亡。CharON 使体内胞葬过程更完整地呈现出来,包括细胞凋亡、吞噬细胞募集、Find、Eat 和 Digest (图6)。通过CharON 还观察到,胚胎果蝇 CNS 中清除凋亡细胞的“重任”由具有吞噬功能的神经胶质细胞和分散的腹侧血细胞 (巨噬细胞) 共同承担。并且还观察到神经胶质细胞和巨噬细胞中吞噬体的大小也有差异,巨噬细胞中凋亡细胞的荧光更密集。 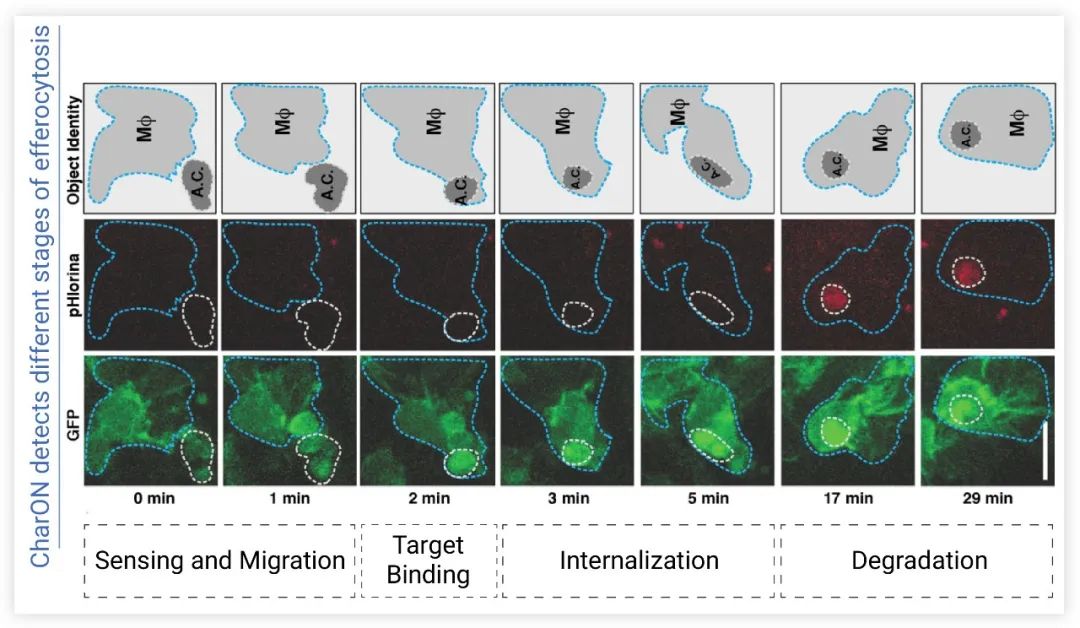
图 6. CharON 可视化果蝇胚胎内胞葬作用的不同阶段[4]
0~1 min:凋亡细胞募集巨噬细胞;2 min:凋亡细胞与巨噬细胞结合;3~5 min:巨噬细胞吞噬。MΦ (蓝色虚线轮廓):GFP 标记的巨噬细胞;A.C. (虚线轮廓):凋亡细胞。细胞凋亡诱导 pH-CaspGFP (绿色) 激活和巨噬细胞 (绿色) 迁移,靶标与受体结合后被吞噬,消化后通过增加 pHlorina 信号 (红色) 检测凋亡细胞的酸化/降解
总结
胞葬作用涉及多个信号通路,包括受体网络、细胞溶质信号分子、细胞骨架快速重排、凋亡细胞消化和免疫代谢通路。这些通路运行不畅则有可能导致多种胞葬缺陷相关疾病(神经退行性疾病、视网膜变性、动脉粥样硬化、癌症等),因此了解胞葬作用机制对于治疗这些疾病更有重要意义。尽管研究之路还很漫长,但相信总有一天我们能攻破难题~
MCE 的所有产品仅用作科学研究或药证申报,我们不为任何个人用途提供产品和服务
参考文献 1. Parul Mehrotra, Kodi S. Ravichandran. Drugging the efferocytosisprocess: concepts and opportunities. Nat Rev Drug Discov. 2022; 21(8): 601-620. 2. Emilio Boada-Romero, et al. Mechanisms and physiology of the clearanceof dead cells by efferocytosis. Nat Rev Mol Cell Biol. 2020 Jul; 21(7):398-414. 3. Evans AL, Heit B, et al. Quantitative Efferocytosis Assays. Methods MolBiol. 2017;1519:25-41. 4. Raymond MH, Ravichandran KS, et al. Live cell tracking of macrophageefferocytosis during Drosophila embryo development in vivo. Science. 2022 Mar11;375(6585):1182-1187.
|