|
|
登陆查看更多优秀资源帖,与同道便捷交流讨论
您需要 登录 才可以下载或查看,没有帐号?立即注册
x
来源:中华病理学杂志
作者:王小桐,倪皓,周晓军,饶秋(南京军区南京总医院病理科 南京医科大学金陵临床医学院)
本文经《中华病理学杂志》授权发布,其他媒体转载或引用须经《中华病理学杂志》同意,否则追究法律责任。
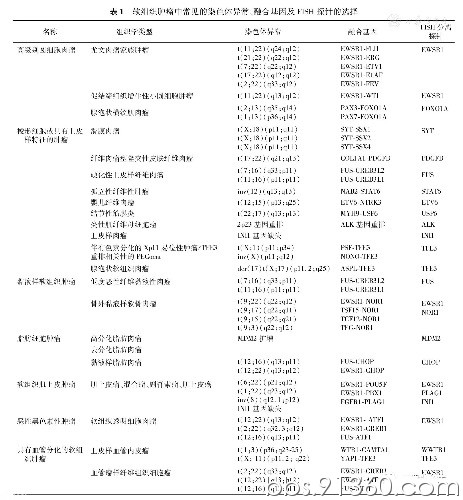
软组织肿瘤是一组高度异质性的肿瘤,有时鉴别诊断十分困难。约1/3的软组织肿瘤都有特征性的分子改变,例如尤文肉瘤/原始神经外胚叶肿瘤(ES/PNET)、脂肪肉瘤、滑膜肉瘤、腺泡状软组织肉瘤等[1,2,3,4]。荧光原位杂交(FISH)作为一种稳定、可靠、简便的分子遗传学检测技术,也成为诊断软组织肿瘤中非常实用的辅助诊断手段。我们综述FISH在诊断软组织肿瘤中的应用,主要包括高级别圆细胞肉瘤、梭形细胞或伴有上皮样特征的肿瘤、黏液样软组织肿瘤、脂肪细胞肿瘤、软组织肌上皮肿瘤、恶性黑色素性肿瘤以及具有血管分化的软组织肿瘤这几大类(表1)。
一、高级别圆细胞肉瘤(high-grade round cell sarcomas)
1.尤文肉瘤家族肿瘤(Ewing family tumor):
是一组高度恶性的小圆细胞肿瘤,包括尤文肉瘤、原始神经外胚叶瘤和Askin瘤。青少年或年轻成人多见,多累及四肢深部软组织。典型的组织学形态是小圆细胞呈片状或小叶状排列,有时具有“菊形团”样结构,有一些肿瘤可表现为不典型形态,比如核增大、核轮廓不规则,梭形细胞、造釉细胞瘤样结构或间质明显硬化,容易和滑膜肉瘤、促结缔组织增生性小圆细胞肿瘤、硬化型上皮样纤维肉瘤或硬化型横纹肌肉瘤混淆。免疫组织化学上,绝大多数表达CD99、FLI1,部分表达突触素、神经元特异性烯醇化酶(NSE)、嗜铬素粒A(CgA)、CD56等神经源性标志物,个别表达细胞角蛋白(CK)和S-100蛋白。分子遗传学上,尤文肉瘤家族肿瘤的定义性特征是存在非随机染色体易位,多涉及位于22q12位点的EWSR1基因与转录因子ETS家族基因(FLI1、ERG、ETV1、ETV4、FEV、ZEG)之一的融合,其中以t(11;22)(q24;q12)形成的EWSR1-FLI1最多见,约占90%;其次是t(21;22)(q22;q12)形成的EWSR1-ERG,约占5%~10%;还有不到5%会发生t(7;22)(p22;q12)形成的EWSR1-ETV1、t(17;22)(q21;q12)形成的EWSR1-ETV4、t(2;22)(q35;q12)形成的EWSR1-FEV、inv(22)(q12;q12)形成的EWSR1-ZSG。这些融合都发生在EWS基因的第1~7号内含子和ETS相关基因第3到9号内含子之间。FUS和EWSR1具有高度同源性,少数病例也可以发生FUS基因代替EWSR1基因与ERG、FEV融合[1,5]。单一的EWSR1分离探针就可以涵盖不同的融合基因类型,可作为诊断尤文肉瘤家族肿瘤的重要辅助依据。在FISH检测EWSR1阴性结果时,可后续检测FUS基因。
2.促结缔组织增生性小圆细胞肿瘤(desmoplastic small round cell tumor):
是一种具有高度侵袭性的恶性肿瘤,好发于年轻男性,多累及腹部、盆腔、腹膜后。组织学上,未分化肿瘤细胞巢被大量致密纤维间质包绕、分隔,瘤巢中央可见坏死,肿瘤细胞分化差,细胞核小而深染,核仁不明显,胞质稀少。免疫组织化学上,表达上皮性标志物[CAM5.2和上皮细胞膜抗原(EMA)]、间叶性标志物(波形蛋白和actin)及神经标志物(NSE和突触素)。结蛋白核周点状分布是该肿瘤所特有的表达方式,WT1通常为弥漫强阳性[1]。肿瘤具有独特的分子遗传学异常t(11;22)(p13;q12),形成EWS-WT1融合基因,存在于90%以上的病例中。通常EWSR1的第7号外显子和WT1的第8号外显子之间融合,EWSR1的活化域和WT1的结合域结合,形成异常的转录因子。FISH对于检测其分子异常具有一定敏感性,逆转录-聚合酶链反应(RT-PCR)也可以确定EWSR1的融合基因。
3.腺泡状横纹肌肉瘤(alveolar rhabdomyosarcoma):
为横纹肌肉瘤的第2常见亚型,发病年龄比其他亚型稍大,好发于四肢深部软组织。组织学上,低分化的圆形或卵圆形细胞聚集,形成“腺泡”样结构,中心的细胞缺乏黏附性,周围由致密的透明纤维间隔分隔包绕。腺泡状横纹肌肉瘤也有“实性”型,缺乏腺泡样结构。80%的腺泡状横纹肌肉瘤含有t(2;13)(q35;q14)形成的PAX3-FOXO1A融合基因或t(1;13)(p36;q14)形成的PAX7-FOXO1A融合基因,前者更常见(70%)[1,6]。PAX3与PAX7是具有高度同源性的转录因子。使用FOXO1A分离探针就可以检测到这2种易位形式,既能为诊断提供依据,也能提示预后。初步研究表明PAX7-FOXO1A比PAX3-FOXO1A预后好[1]。值得注意的是,约20%病例不存在基因异常,因此FISH结果阴性时也不能排除腺泡状软组织肉瘤的诊断。
二、梭形细胞或具有上皮样特征的肿瘤
1.滑膜肉瘤(synovial sarcoma):
滑膜肉瘤是青壮年常见的软组织肿瘤,约占软组织肉瘤的5%~10%,好发于四肢大关节附近,常与腱鞘、滑囊及关节囊紧密相关。组织学上主要分为2种类型:双相型和单相型。双相型滑膜肉瘤含有比例不等的上皮样细胞和梭形细胞成分,单相型滑膜肉瘤又分为单相纤维型和单相上皮型。单相上皮型和低分化滑膜肉瘤是诊断的难点,95%以上的滑膜肉瘤存在t(X;18)(p11;q11)平衡易位,导致第18号染色体上SYT(SS18)基因与X染色体上SSX基因(SSX1、SSX2、SSX4)产生融合。一些研究发现融合类型和肿瘤组织学相关,大多数携带SYT-SSX2的肿瘤为单相型滑膜肉瘤,而双相型滑膜肉瘤则多为SYT-SSX1融合[1]。
2.隆突性皮肤纤维肉瘤(dermatofibrosarcoma protuberans):
是一种发生于真皮内的中间型纤维组织细胞肿瘤,也可发生于深部软组织,浸润性生长,但很少发生转移。组织学亚型较多,其中少数可出现高级别纤维肉瘤样改变,当纤维肉瘤成分超过5%时,则称为纤维肉瘤型隆突性皮肤纤维肉瘤[7],其临床、病理以及生物学行为与其他亚型不同,具有较高的侵袭性,复发率和转移率显著高于经典型隆突性皮肤纤维肉瘤。纤维肉瘤型和经典型具有相同的遗传学改变,特异性的染色体易位t(17;22)(q21;q13),产生COL1A1-PDGFB融合基因。
3.孤立性纤维性肿瘤(solitary fibrous tumor, SFT):
是一种较为少见的间叶细胞来源的肿瘤,主要发生在成年人,可广泛发生在身体任何部位。虽然多数SFT为孤立性生长,但是局部复发率和/或转移率仍达10%~15%。镜下可见肿瘤细胞稀少区和丰富区交替分布。瘤细胞间有粗大的玻璃样变胶原和分支状血管外周细胞瘤样血管分隔。有些病例还有黏液变和纤维化。免疫表型上,SFT特征性表达CD34和CD99,也可不同程度的表达EMA、bcl-2、平滑肌肌动蛋白(SMA)。对SFT进行大规模测序研究发现染色体内易位inv(12)(q13;q13),形成NAB2-STAT6融合基因(主要有3种融合形式:NAB2ex4-STAT6ex2、NAB2ex6-STAT6ex16以及NAB2ex6-STAT6ex17)驱动STAT6核表达[8,9]。已经有研究发现STAT6的表达对于鉴别诊断SFT具有较高的敏感性和特异性[9]。FISH检测SFT中融合基因发生在同一个染色体上2个相邻基因中,FISH结果中红、绿信号分离并不明显,可能出现假阴性结果,因此在选用RT-PCR检测该融合基因更为合适。
4.婴儿纤维肉瘤(infantile fibrosarcoma):
又称为先天性纤维肉瘤,是一种少见低度恶性的软组织肉瘤,预后较好。常发生于1岁以内的婴儿,好发于四肢末端软组织。其组织学形态与成人型纤维肉瘤相似,但细胞更为幼稚,缺乏多核及巨核瘤细胞;有慢性炎性细胞浸润;血管丰富,类似血管肉瘤及血管外皮瘤样结构。婴儿纤维肉瘤具有特异性的染色体易位t(12;15)(p13;q25),该易位引起位于12p13的ETV6基因与位于15q25的NTRK3基因融合[10,11]。
5.结节性筋膜炎(nodular fasciitis):
是一种常见的反应性结节性肌纤维母细胞增生性的自限性病变,多见于年轻人。镜下可见增生活跃的肌纤维母细胞呈席纹状、旋涡状或结节状排列,间质水肿和黏液变,新生的毛细血管和红细胞外渗现象,常常缺乏特异性的标志物。分子遗传学方面,USP6基因重排是结节性筋膜炎一种常见的遗传学改变,多涉及t(22;17)(q13;p13),形成MYH9-USP6融合基因[12]。USP6基因重排还见于原发性动脉瘤样骨囊肿中,而在其他梭形细胞软组织肿瘤中并未发现。
6.炎性肌纤维母细胞瘤(inflammatory myofibroblastic tumor,IMT):
好发于儿童和少年,最常累及网膜、腹膜后、盆腔和腹部软组织,其次是肺、纵隔等。IMT是一种中间型肿瘤,组织学形态多样,主要由增生的纤维母细胞、肌纤维母细胞构成,其间可见数量不等的炎细胞浸润。分子遗传学方面,约50%的IMT具有ALK基因(位于2p23)的克隆性重排,目前发现的ALK基因的伙伴基因有CLTL、TPM3、TPM4、CARS、ATIC、SEC31L1、RANBP2[13]。ALK基因的克隆性重排导致ALK蛋白的激活表达,因此约50%~60%的病例瘤细胞呈ALK蛋白阳性表达。FISH技术采用ALK分离探针可以检测该基因重排。
7.上皮样肉瘤(epithelioid sarcoma):
是组织来源不明的间叶肿瘤,恶性程度高,常常复发或转移,预后较差。其主要分为两种类型:经典型和近端型。经典型上皮样肉瘤主要发生于肢体远端,由上皮样细胞和梭形细胞构成;近端型常位于会阴、外生殖区及躯干,由上皮样细胞及横纹肌样细胞构成,细胞异性明显,更具侵袭性。近年来发现INI1蛋白在其中表达缺失,但在很多与上皮样肉瘤形态学交叉的肿瘤中仍然保留,因此使用免疫组织化学INI1在上皮样肉瘤的鉴别诊断中显得非常重要。使用INI1基因FISH探针也可以检测上皮样肉瘤中的基因缺失:荧光显微镜下,一个正常细胞核内有红、绿信号各有2个,当细胞核内红绿信号各有1个时即为单倍体;当细胞核内2个绿信号和1个红信号时,为INI1基因杂合性缺失;细胞核内仅有2个绿信号,无红信号时,为INI1基因纯合性缺失[14]。
8.伴有色素分化的Xp11易位性肿瘤/TFE3重排相关性的PEComa(Xp11 neoplasm with melanocytic differentiation/ TFE3 rearrangement-associated perivascular epithelioid cell tumors):
这一类肿瘤的形态特征、免疫表型、分子遗传学、预后都不同于传统的PEComa,但跟伴有色素分化的TFE3易位性的肾细胞癌相同,因此有报道认为两者属于一个单独的病理谱系,因此建议以伴有色素分化的Xp11易位性肿瘤来命名这类肿瘤[15,16]。这类肿瘤女性患者多于男性,儿童或年轻人多见,偶见于老年人,可发生于全身多个脏器,如肾、前列腺、子宫、宫颈、结肠、胰腺等。镜下肿瘤由纤维血管分隔呈巢状或片状分布,缺乏乳头状结构,肿瘤细胞主要由上皮样细胞组成,圆形、卵圆形,胞质透明至嗜酸,核仁可见,缺乏梭形细胞和脂肪成分。免疫表型上,这类肿瘤表达TFE3、Cathepsin K、HMB45、Melan A,而肌源性标志物(SMA和结蛋白)、上皮性标志物(广谱CK和EMA)、肾小管标志物(CD10、PAX2、PAX8)、神经源性标志物(S-100蛋白)均不表达。分子遗传学上具有特征性的Xp11易位,形成PSF-TFE3、NONO-TFE3融合基因,前者最为常见[15],后者很罕见,目前在这类肿瘤只发现过1例[16]。采用TFE3分离探针进行FISH检测可以有效检测出Xp11易位。
9.腺泡状软组织肉瘤(alveolar soft part sarcoma):
多发生于儿童和青年,女性患者显著多于男性,好发于臀部和大腿软组织。组织学上,肿瘤由薄壁窦状血管腔分隔成巢状或腺泡状,瘤细胞较大,呈圆形或多角形,胞质丰富,半透明空泡状或嗜伊红颗粒状。免疫组织化学通常表达SMA、TFE3,偶尔表达S-100蛋白,其中TFE3免疫组织化学检测对于腺泡状软组织肿瘤具有一定的特异性。分子遗传学上,该肿瘤存在特异性基因非平衡易位,即der(17)t(X;17)(p11.2;q25),形成ASPL-TFE3基因[17,18]。对于发病部位少见的不典型病例或在细针穿刺活检组织较少的情况,有时镜下形态与分化较为原始的胚胎性横纹肌肉瘤较难区分,诊断更加难以明确,采用TFE3分离/断裂探针的FISH方法,可以将该肿瘤与副神经节瘤、颗粒细胞瘤鉴别开来。Xp11.2易位相关性肾癌也存在TFE3基因重排,采用TFE3分离探针,结果也为阳性,但腺泡状软组织肉瘤表达SMA,不表达肾小管标志物,因此容易鉴别。
三、黏液样软组织肿瘤(myxoid soft tissue neoplasms)
1.低度恶性纤维黏液性肉瘤(low-grade fibromyxoid sarcoma):
多累及深部软组织,形态上纤维区域和黏液区域交错混合,有时会出现梭形细胞和玻璃样间质形成的巨大“菊形团”样外观,瘤细胞相对温和,核分裂象少见。约2/3的病例存在特征性的分子遗传学异常t(7;16)(q33;p11),约1/4会形成冗环染色体,这两种畸变都形成FUS-CREB3L2融合基因[19]。另外还有一种遗传学异常t(11;16)(p11;p11),形成FUS-CREB3L1融合基因,占4%~6%[20]。在个别病例中出现EWSR1替换FUS与CREB3L2或CREB3L1发生融合[21]。有研究发现,硬化性上皮样纤维肉瘤和低度恶性纤维黏液性肉瘤在形态上和分子遗传学上都有一定交叉,前者也存在t(7;16)(q33;p11)和t(11;16)(p11;p11)这2种易位形式。MUC4已被发现是诊断低度恶性纤维黏液性肉瘤的敏感性和特异性的标志物,而78%的硬化性上皮样纤维肉瘤也表达MUC4蛋白,MUC4表达跟FUS基因重排有关[22]。有研究认为MUC4阳性且具有FUS基因重排的硬化性上皮样纤维肉瘤更接近于低度恶性纤维黏液性肉瘤[22,23]。
2.骨外黏液样软骨肉瘤(extraskeletal myxoid chondrosarcoma):
是一种较为罕见的肉瘤,形态上呈多结节状,由形态大小较一致的圆形或椭圆形细胞组成。在免疫组织化学表达上没有特异性的标志物,20%~50%病例S-100蛋白灶状阳性或弱阳性,30%病例CD117阳性,还有部分病例表达EMA和神经内分泌标志物。分子遗传学上骨外黏液样软骨肉瘤存在特征性的染色体易位,最常见的是t(9;22)(q22;q12),形成EWSR1-NOR1融合基因(也称为NR4A3、TEC、CHN);另外大约15%的病例存在t(9;17)(q22;q11),形成TAF15-NOR1融合基因[24];还有个别病例报道了t(3;9)(q12;q22)、t(9;15)(q22;q21)分别形成TFG-NOR1和TCF12-NOR1融合基因。FISH技术使用NOR1分离探针就可以测出上述几种易位,但这个探针目前还没有广泛投入使用。
四、脂肪细胞肿瘤(adipocytic neoplasms)
WHO将其分为5种类型,包括不典型脂肪瘤性肿瘤/高分化脂肪肉瘤、去分化脂肪肉瘤、黏液样脂肪肉瘤、多形性脂肪肉瘤和混合型脂肪肉瘤。其中,高分化脂肪肉瘤和去分化脂肪肉瘤是最常见的类型,约占40%~50%,并具有特征性的巨大染色体或环状染色体含有扩增的12q13-15的片段,该片段含有几个基因(如MDM2、GLI、SAS、CDK4和HMGIC),这种结构异常导致MDM2扩增,附近的GLI、SAS、CDK4和HMGIC基因也常常出现扩增。另一种常见的类型就是黏液样脂肪肉瘤,大于95%都具有t(12;16)(q13;p11),形成FUS-CHOP融合基因。MDM2基因探针可以用来鉴别高分化脂肪肉瘤和脂肪瘤(尤其是当脂肪瘤发生在深部,含有明显的纤维分隔或明显的黏液成分时)[25,26],脂肪瘤中也有12q13-15易位,但不扩增。FISH检测也可用于高分化脂肪肉瘤和多形性脂肪肉瘤的鉴别诊断中,后者不具有MDM2基因扩增[27]。对于去分化脂肪肉瘤而言,MDM2探针缺乏特异性但敏感性较高。在黏液样脂肪肉瘤中,大于95%具有FUS-CHOP融合基因。FUS编码一个RNA结合蛋白,类似于EWSR1蛋白,而CHOP是一个转录因子,参与脂肪细胞分化过程。由于FUS基因和EWSR1基因具有高度相关性,因此有一小部分病例存在t(12;22)(q13;p12),形成EWSR1-CHOP融合基因[28]。FUS基因重排也会发生在低级别纤维黏液样肉瘤,而CHOP基因重排目前只发生在黏液样脂肪肉瘤中。评估时最有效的方法就是用CHOP探针进行FISH检测,既可以测到t(12;16),也可以测到t(12;22)。相反如果使用FUS探针就容易和低级别纤维黏液性肉瘤混淆,还有一部分病例会出现假阴性结果。而圆形细胞为主的黏液样脂肪肉瘤也可能存在EWSR1基因重排,需要与同样具有EWSR1基因重排的ES/PNET进行鉴别,利用CD99可以鉴别,CD99在ES/PNET中阳性表达,而在黏液样脂肪肉瘤中不表达。
五、软组织肌上皮肿瘤(myoepithelial tumors of soft tissue)
软组织肌上皮肿瘤包括肌上皮瘤、混合瘤、副脊索瘤以及恶性的肌上皮癌。这些肿瘤多累及肢体、躯干的深部软组织。镜下肿瘤组织结构和细胞形态多样。约90%的病例表达CK、S-100蛋白、calponin,60%表达EMA。分子遗传学上,肌上皮肿瘤存在多种基因异常,EWSR1基因的易位较为常见(45%),包括t(6;22)(p21;q12)和t(1;22)(q23;q12)两种易位形式,分别形成EWSR1-POU5F和EWSR1-PBX1融合基因[29]。和上述涉及EWSR1基因易位的肿瘤一样,少数病例可发生FUS基因取代EWSR1基因易位[28]。涉及EWSR1基因易位的肌上皮肿瘤中超过一半组织学上显示恶性,而不涉及EWSR1基因易位的肌上皮肿瘤通常为良性,发生在浅表部位,形态上往往有腺管分化,在基因遗传学上多累及位于8q12.1上的PLAG1基因,易位形式尚无定论,曾经报道过inv(8)(q12.1;p12)易位形成FGFR1-PLAG1融合基因[30]。还有部分肌上皮癌会出现INI1基因缺失。
六、恶性黑色素性肿瘤:软组织透明细胞肉瘤(clear cell sarcoma of soft parts)
软组织透明细胞肉瘤是一种具有黑色素分化的肉瘤,主要发生在皮下或深部软组织,很少累及皮肤。常常需要和原发或转移性黑色素瘤、腺泡软组织肉瘤进行鉴别。透明细胞肉瘤具有特殊的染色体易位t(12;22)(q13;q12),产生EWSR1-ATF1融合基因,约占90%;还有部分发生t(2;22)(q32.3;q12)形成EWSR1-CREB1,约占6%;以及少量t(12;16)(q13;p11)形成FUS-ATF1[31]。ATF1/EWSR1与小眼转录因子的启动子结合,在黑色素分化的过程中起着重要作用。EWSR1探针对于鉴别诊断透明细胞肉瘤具有高度敏感性,可以用来检测其中出现的t(12;22)和t(2;22)。尽管很多肿瘤都涉及这种EWSR1易位,但黑色素瘤中未发现。
七、具有血管分化的软组织肿瘤
1.上皮样血管内皮瘤(epithelioid haemangioendothelioma, EHE):
是一种较为罕见的恶性血管源性肿瘤,多发生于软组织,也可发生于实质脏器。组织学形态上,瘤细胞呈条索状或小巢状排列,分布于黏液样或玻璃样基质中,其间有大小不等的小血管腔隙。表达多种血管内皮抗原:CD31、CD34、FLI1、ERG、第Ⅷ因子相关抗原,但这些血管标志物在鉴别其他血管源性肿瘤时不具有特异性。分子遗传学方面,绝大多数的EHE都存在t(1;3)(p36;q23-25),导致位于3q23-24的WWTR1基因与1p36的CAMTA1基因的易位,形成WWTR1-CAMTA1融合基因[32],这是EHE特异性的染色体平衡易位,目前尚未在其他软组织肿瘤中检测到此类融合基因的存在,因此采用WWTR1分离探针FISH检测这种特异性染色体异常会成为EHE有力的辅助诊断。近来,在该肿瘤中又发现有少数病例存在Xp11易位,导致TFE3基因与YAP1融合,形成YAP1-TFE3融合基因[33]。在FISH检测WWTR1阴性结果时,可后续检测TFE3基因。
2.血管瘤样纤维组织细胞瘤(angiomatiod fibrous histiocytoma):
主要发生于儿童和青少年,常表现为无痛性软组织包块,多累及四肢、躯干和头颈的皮下部位,也可发生于脏器和深部软组织。该肿瘤很少转移,临床预后良好。镜下形态有3个特征:组织细胞样细胞结节状分布、囊性出血区、慢性炎细胞浸润形成致密的外周袖套并与假被膜相互融合。部分病例表达结蛋白、EMA、CD99、CD68,其中结蛋白胞质内树突状阳性是该肿瘤的特征和诊断线索。分子遗传学上,该肿瘤也涉及EWSR1基因重排,最常见的t(2;22)(q33;q12),形成EWSR1-CREB1融合基因(90%),其次是t(12;22)(q13;q12)形成的EWSR1-ATF1[34]。少数发生t(12;16)(q13;p11),形成FUS-ATF1融合基因。
上述肿瘤使用FISH方法均可在很大程度上帮助我们进行鉴别诊断,但是也存在一些问题,例如涉及EWSR1基因重排的软组织肿瘤很多,因此在判读FISH结果时也需要结合形态学和免疫组织化学作为基础,同时需要了解患者的病史信息,进行综合分析才能做出最适合的正确诊断,并指导后续治疗。
|
-
|