登陆查看更多优秀资源帖,与同道便捷交流讨论
您需要 登录 才可以下载或查看,没有帐号?立即注册
x
性别:男
年龄:60岁
数字病理切片:
[align=center][align=center][align=center]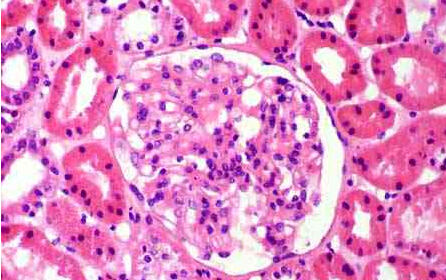 [/align][/align][/align] [/align][/align][/align]
临床资料:患者于1998年12月无明显诱因下出现双下肢凹陷性浮肿,在当地医院检查血压115/75mmHg,尿蛋白1.3g/24h,尿RBC5~10个/HP,Scr85μmol/L,给予雷公藤多甙片60mg/d治疗1月,尿蛋白降至1.0g/d,但因出现轻度贫血(Hb100g/L),白细胞减少至3.10×109/ml,故停用雷公藤。此后尿蛋白波动于1.0~2.85g/24h之间。因持续蛋白尿,病因不明转至我院就诊。病程中患者无长期发热,无腹胀、排便异常,无黑便、鲜血便,无皮疹、关节痛,食欲一直正常,体重无明显减轻。
病史:既往体健,否认糖尿病、结核病史,无疫区居住史,无放射线、毒物接触史,预防接种随社会进行。父母体健,育有4个子女,体健,否认家族性遗传病史。
查体:体温36.7℃,脉搏80次/分,呼吸16次/分,血压120/80mmHg,体重82Kg,身高173cm,无病容,发育正常,营养良好,意识清楚,自动体位。全身皮肤无皮疹、出血点,无黄染,无口腔溃疡,全身浅表淋巴结无压痛、肿大,头颅外形正常,双侧角膜无混浊,巩膜无黄染,对光反射灵敏,鼻腔无异常分泌物,鼻窦无压痛,扁桃体轻度肿大,无化脓,甲状腺不肿大。胸廓正常,呼吸音正常,无干湿罗音,无胸腔积液征,心律齐,心界不扩大,无心脏杂音,无心包摩擦音。腹部饱满,腹壁静脉无曲张,全腹无压痛、反跳痛,肝脾肋下未及,腹水征阴性,未触及包块,肠鸣音正常,四肢关节无肿胀,无压痛,无畸形,活动度正常,双下肢无浮肿。四肢肌力正常,生理反射存在,病理反射未引出。
血常规:Hb100g/L,平均红细胞体积60.2fL(80.00-100.00),平均红细胞血红蛋白量(MCH)20.70pg/L(27.00-33.00),平均红细胞血红蛋白浓度(MCHC)344.00g/L(320.00-360.00),网织红细胞计数6%,WBC3.8×109/L,N 0.68,L 0.32,单核细胞0.08,血小板229×109/L。
尿液学检查:尿蛋白定量3.0g/24小时,尿沉渣RBC4万/ml(多形型),无管型及白细胞尿,尿NAG酶29.2M/g.cr,尿C3及α2m(-)。禁水13小时尿渗量680mOsm/Kg.H2O,尿酸化功能:PH6.2,HCO3-21mmol/L,TA41 mmol/L,NH4 44 mmol/L,NAC64 mmol/L,NH4 /TA1.07。尿本-周蛋白阴性,尿κ、λ链水平正常。
粪常规:隐血阴性。
血生化:胆红素水平正常,白蛋白28.1g/L,球蛋白26.9g/L,谷丙酶15U/L,谷草酶26U/L,碱性磷酸酶68U/L(50-172),BUN5.2mmol/L,Scr89umo/L,Ccr92ml/min/m2,UA359mmol/L,K 4.6mmol/L,Na 142mmol/L,Cl-107mol/L,CO2-CP 25mmol/L,Ca2 2.0mmol/L,磷1.2mmo/L,胆固醇6.4mmol/L,甘油三酯1.48mmol/L,空腹血糖4.6mmol/L,餐后血糖6.1mmol/L,糖化血红蛋白4.7%,血清铁5.9μmol/L(6.6-32),AFP、CEA阴性,血游离κ、λ链水平正常。
血清检查:ANA、A-dsDNA、A-Sm、A-RNP阴性,补体C3 0.89g/L,C4 0.19g/L,总补体活性1:8,循环免疫复合物阴性。HBsAg( ),抗HBcAb( ),HBeAg( ),HBV-DNA(-)。
肾脏B超:左肾104X50.5X51mm,右肾102X46.7X49.5mm,回声正常。肝胆B超正常,ECG示窦性心率,不完全性右束支传导阻滞,胸部X线片检查正常。上消化道钡餐未见异常。
骨髓穿刺细胞学检查示骨髓像增生活跃,白细胞分类各系比例、形态正常,未见浆细胞,成熟红细胞形态正常,铁染色示细胞外铁阴性,细胞内铁Ⅰ型9%,符合缺铁性贫血。
肾活检病理:光镜下一条皮质,20个肾小球,无分叶及硬化,细胞数90个/球,为肾固有细胞,系膜基质节段增生,节段增宽的系膜区中可见3个系膜细胞,袢开放尚好,包囊壁节段增厚。PASM-Masson染色:阴性。小管间质轻度病变,小管腔内蛋白管型。间质散在浸润细胞。动脉无明确病变。刚果红染色阴性,免疫荧光:IgA ,IgM ,C3 ,C4 ,C1q 颗粒状沉积于系膜区及血管袢,IgG(-)。HbcAg、HBeAg、κ、λ链染色均阴性。
初步诊断:肾病综合征,肾小球系膜增生性病变(继发性)。
病情分析:该患者的病情并不复杂,临床有以下特点:1、老年男性;2、表现为肾病综合征,伴少量镜下血尿,肾小管功能损伤轻,血压及肾功能正常;3、增生性小细胞低色素性贫血,伴有缺铁;4、HBV感染,肝功能正常,HBV-DNA(-);5、肾活检示肾小球轻度系膜增生性病变,肾小管间质、血管无病变;6、无糖代谢异常,血、尿轻链水平正常。
根据上述病情待点,临床上需重点排除继发性肾脏病,尤其是肿瘤、淀粉样变性、糖尿病肾病、慢性感染等。患者入院后查糖代谢正常,因此可排除糖尿病肾病。肾脏组织刚果红染色阴性,排除了肾淀粉样变性,肾组织中无轻链沉积,故排除了轻链相关性肾病。肾组织免疫组化染色HBc、HBeAg阴性,不符合乙肝相关性肾病。临床上也排除了自身免疫性疾病。多种影像学检查包括X线胸片、肝胆B超、上消化道钡餐等未发现明确占位性病变。因此临床各项检查未能发现可导至肾病的其它疾病存在。但该患者的贫血(尽管有缺铁证据,临床却无造成缺铁的病因)提示患者的肾脏病并非原发,而是有其它疾病存在。因此初步诊断为肾病综合征,肾小球系膜增生(继发性),治疗上予常规降蛋白尿治疗,同时门诊定期随访,继续寻找可能的病因。
治疗:常规降蛋白尿治疗无效。患者肾活检后临床上未寻找到继发性肾脏病的病因,故先予雷公藤多甙120mg/日(治疗1月后减量为60 mg/日)及洛汀新治疗,并予补铁纠正贫血。门诊随访显示疗效不明显,尿蛋白波动在1.68~4.76g/24小时之间,血清白蛋白31.0g/L左右,Hb在100~109g/L之间,加用血管紧张素Ⅱ受体拮抗剂(科素亚)治疗2月后,尿蛋白仍无改善。2000年3月停用雷公藤多甙,予强的松诱导治疗(60mg/d),4周后尿蛋白仍无下降,4.35g/24小时,隧逐渐减撤强的松至停药。至此,尽管患者肾脏病理改变较轻,但雷公藤、ACEI联合ARB及足量强的松治疗却无效,贫血持继存在。
因小肠穿孔发现小肠肿瘤。2000年6月患者因突然出现右下腹剧痛,6小时后在当地医院急诊行剖腹探查术,术中查见距回盲部130cm处约8×9cm2的小肠肿块,边缘有穿孔形成,孔径约10mm,有粪质流出,阑尾正常。肿块切除后病理证实为小肠肠道间质瘤,向神经鞘瘤分化,低度恶性,累及浆膜层,切缘未见瘤组织,术后未行放疗或化疗,同时停用洛丁新等治疗。
小肠肿瘤病灶切除后蛋白尿逐渐下降直至完全缓解。术后4月(2000年10月)复查尿蛋白下降至2.79g/d,血白蛋白上升至33.0g/L,术后6月时复查尿蛋白降至0.51g/d,血白蛋白升至36.0g/L,Hb升至121g/L,术后一年尿蛋白0.43g/d,血浆蛋白升至43.0g/d,血色素升至129g/L。至今患者尿蛋白持继阴性。
纵观患者整个病程,在原发病去除后,尿蛋白消失,贫血纠正,完全支持患者肾小球病变与小肠间质瘤有关。
讨论:本例由于早期缺乏肠道肿瘤的症状,仅表现为单纯蛋白尿,因而造成原发病的延迟诊断。除肿瘤易被漏诊外,轻链相关的肾病(如不典型的淀粉样变性)、基因缺陷所致的肾脏病(如Alport综合征、薄基底膜肾病)、临床不典型的自身免疫性疾病也是容易被误诊为“膜增生性肾炎”。需要注意的是某些肿瘤相关性肾病激素治疗也有效,可见对系膜增生性病变的病例,应积极寻找各种可能的病因,而不能单凭激素治疗反应来判断原发或继发性肾病。在临床上我们还曾经遇到一例镜下血尿的患者,外院肾活检诊断为肾小球系膜增生性肾炎,至我院重复肾活检并作肾组织胶原IVα3、α5链染色,证明肾小球基底膜胶原IVα5链缺失,确诊为Alport综合征。因此详细的临床检查,结合肾组织特殊病理检测如刚果红及轻链染色(排除淀粉样变性)、胶原IVα3、α5链染色(有助于诊断Alport综合征),电镜检查以及长期随访对明确肾小球系膜增生的病因很有帮助。对不同的病人根据临床特点有选择地进行上述检查,例如老年患者则应该重点排除肿瘤、轻链相关的肾病,对儿童及青少年患者则应排除Alport综合征等。
【本站为非盈利学术交流平台,部分资料来源于网络,如涉及版权问题请及时联系管理员处理;所有文章仅供公益交流,不代表本站立场。欢迎提供素材、资料等,一经采纳将给予稿费。】
|