登陆查看更多优秀资源帖,与同道便捷交流讨论
您需要 登录 才可以下载或查看,没有帐号?立即注册
x
患者55岁,男性,因颈部肿块,逐渐变大就诊
大体:灰红组织一块,大小5*4*3cm,切面见一肿块,大小1.8*1cm,灰白质中,界限欠清。
[align=center][align=center][align=center] 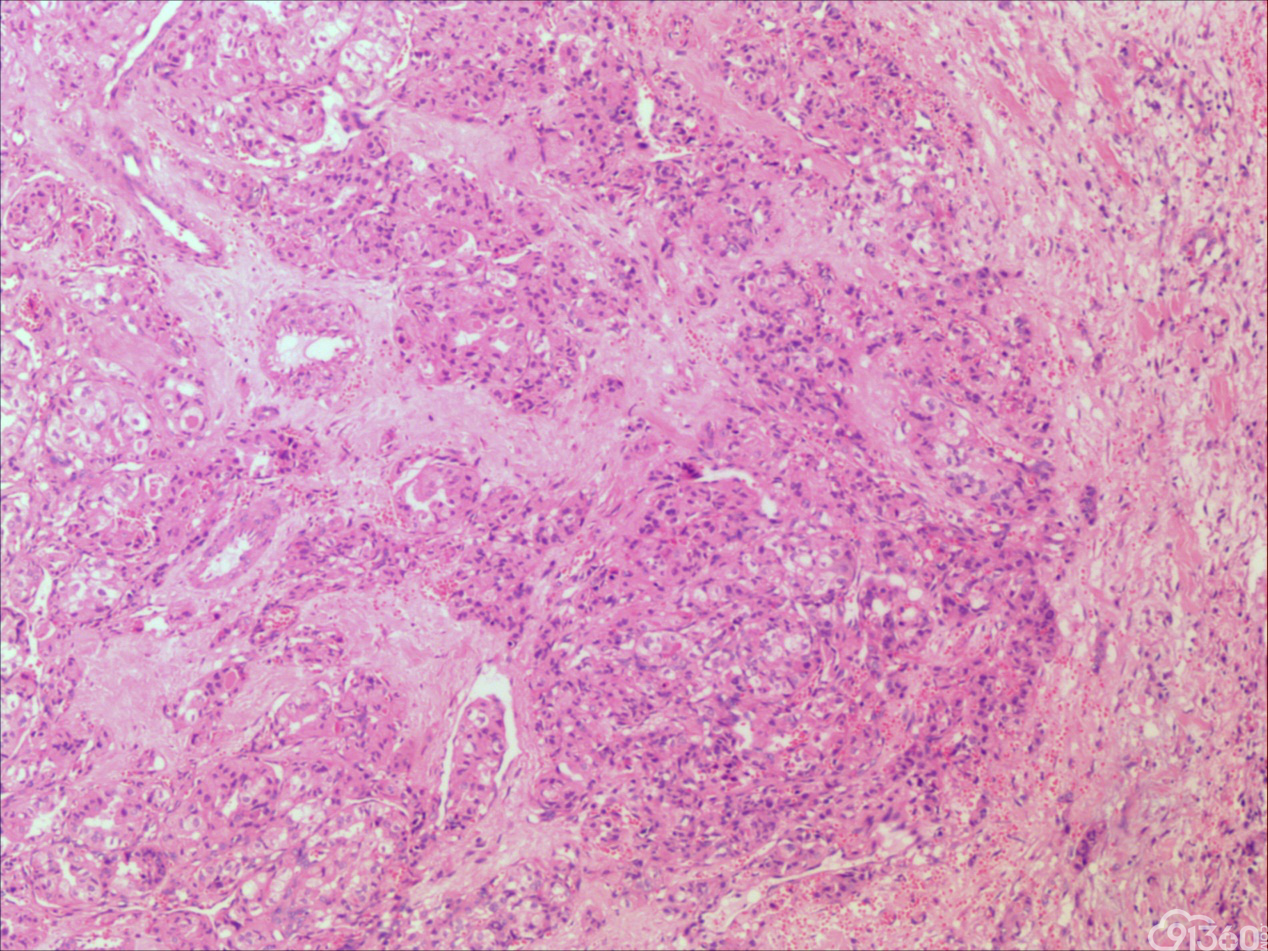 [/align][/align][/align]
[align=center][align=center][align=center] 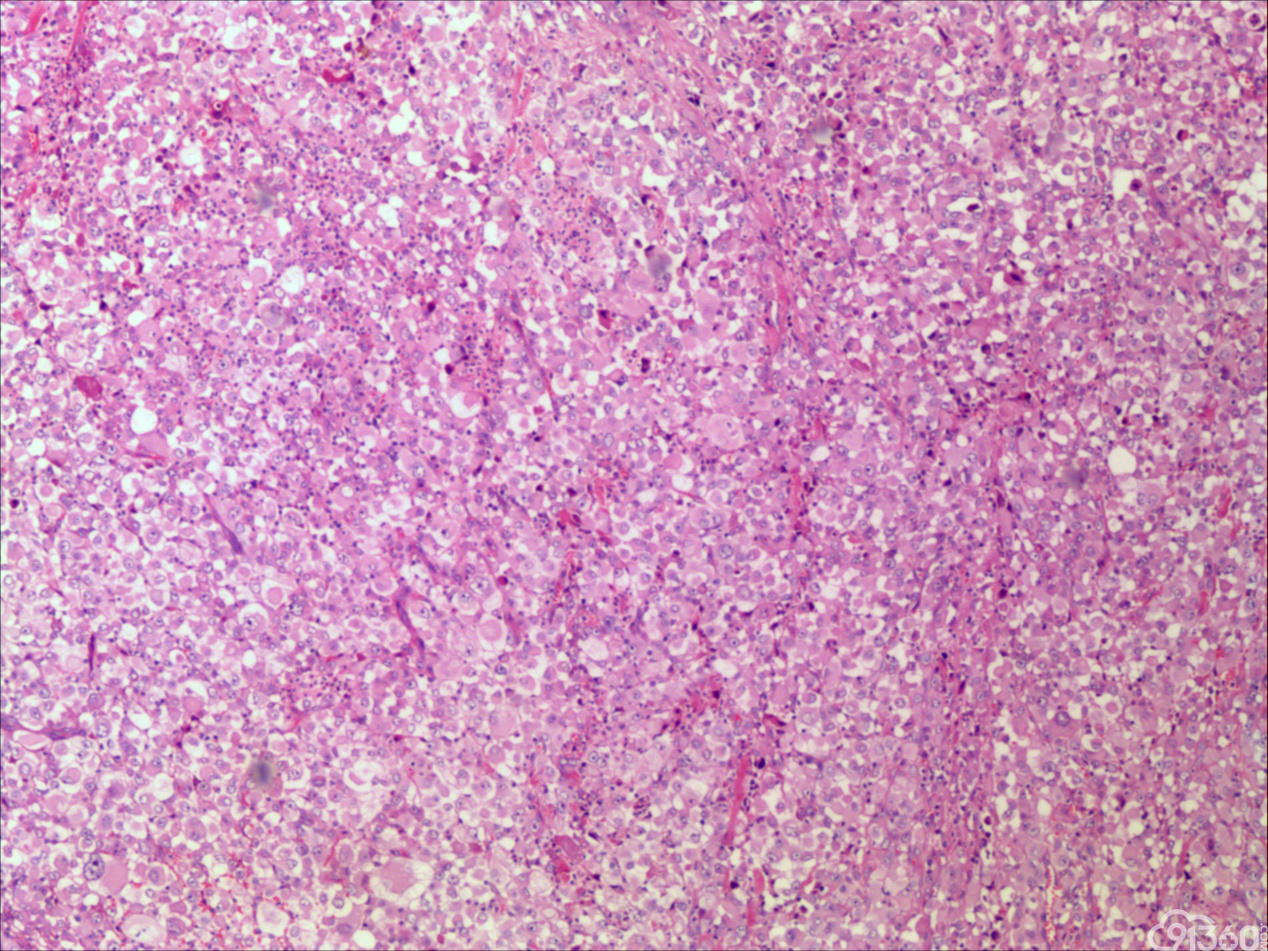 [/align][/align][/align]
[align=center][align=center][align=center] 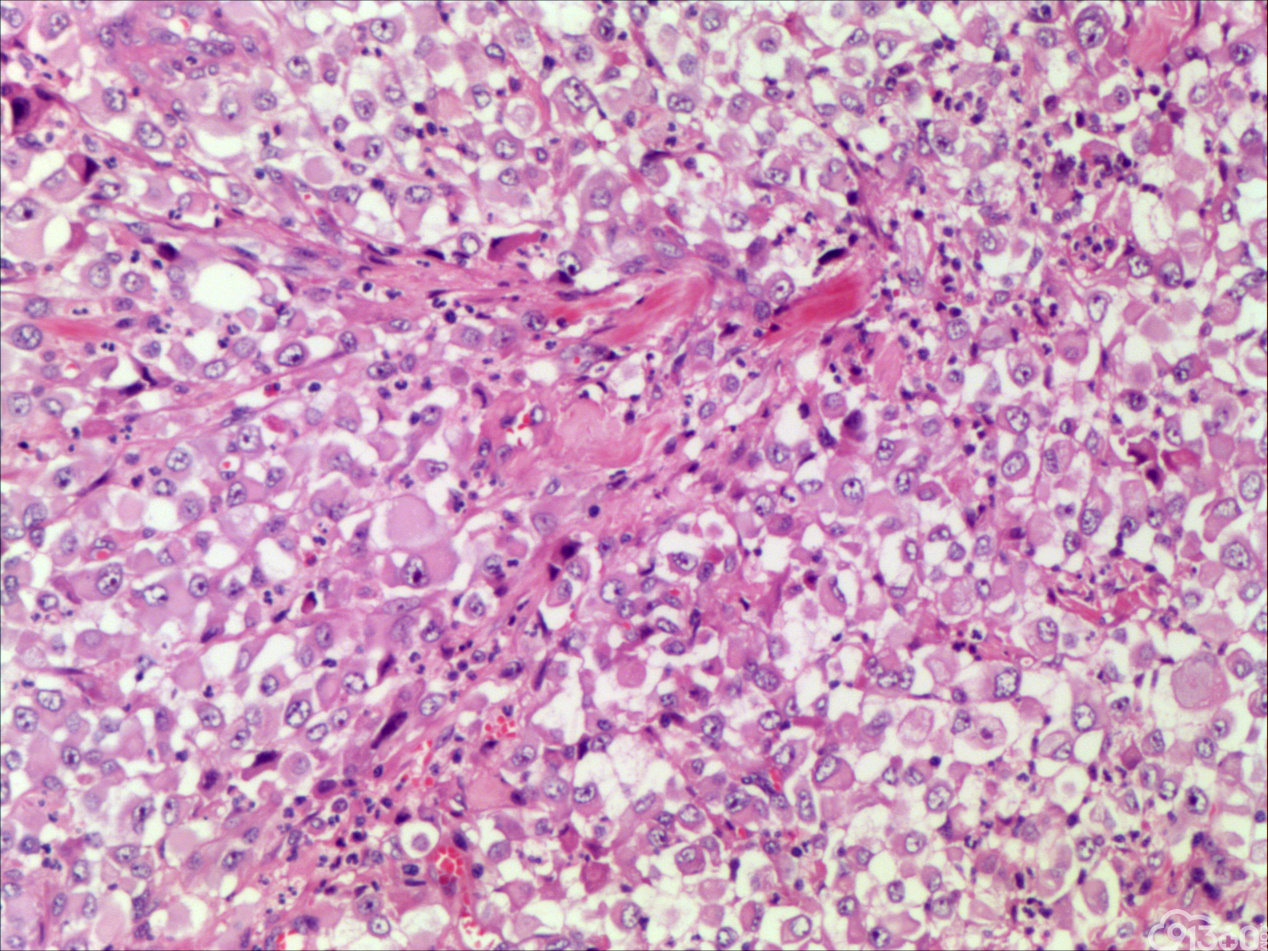 [/align][/align][/align]
[align=center][align=center][align=center] 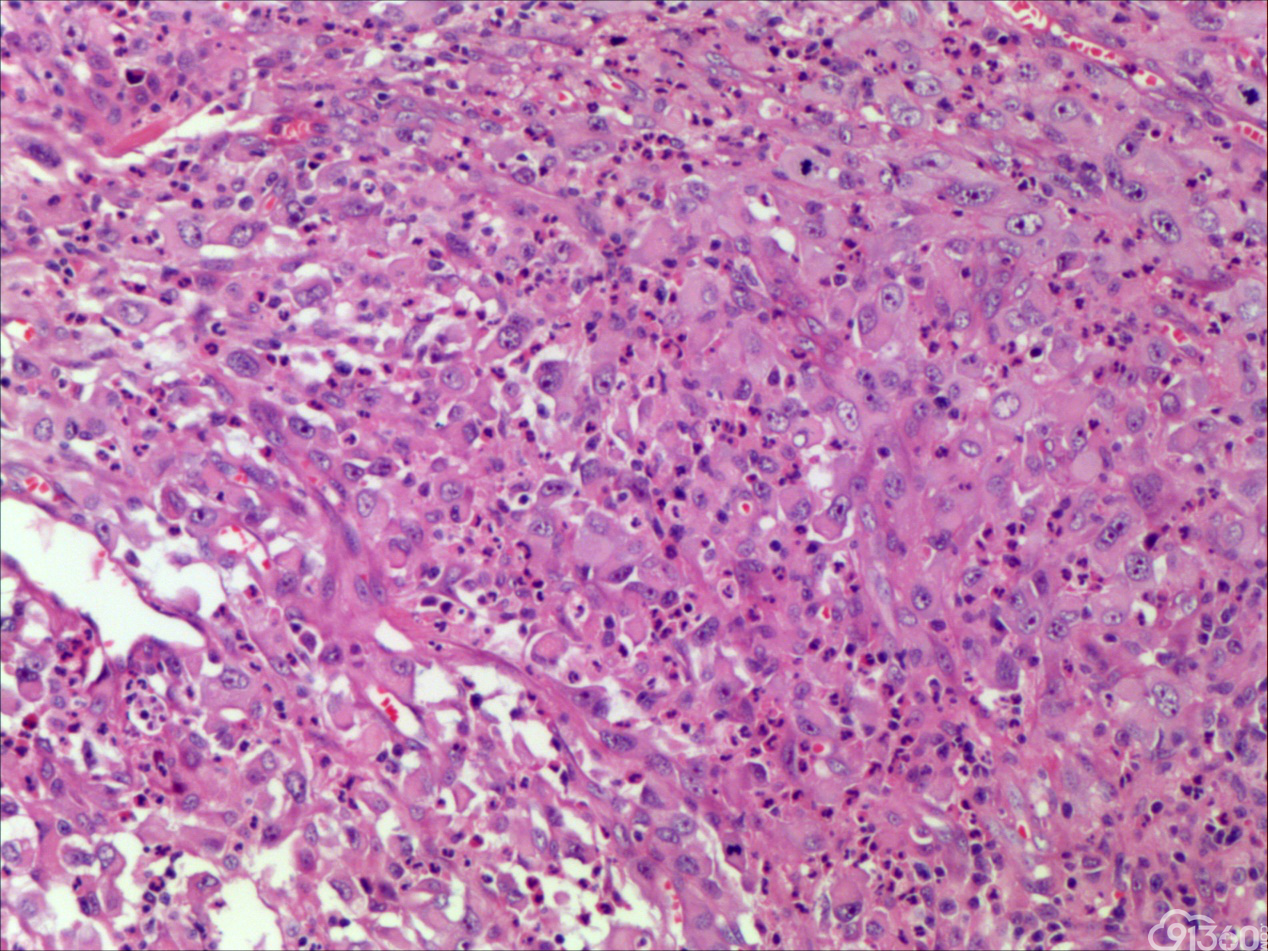 [/align][/align][/align]
[align=center][align=center][align=center] 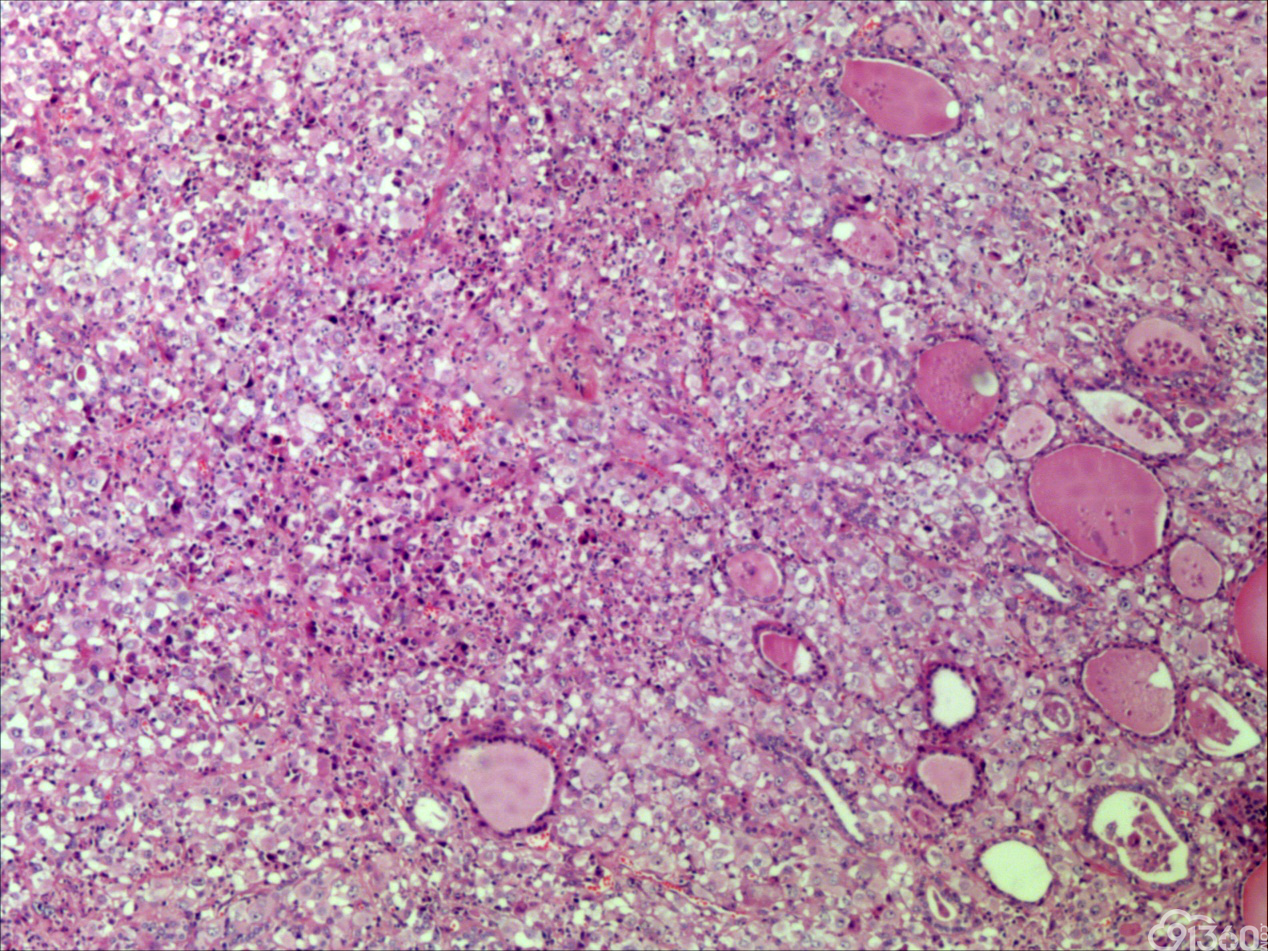 [/align][/align][/align]
[align=center][align=center][align=center] 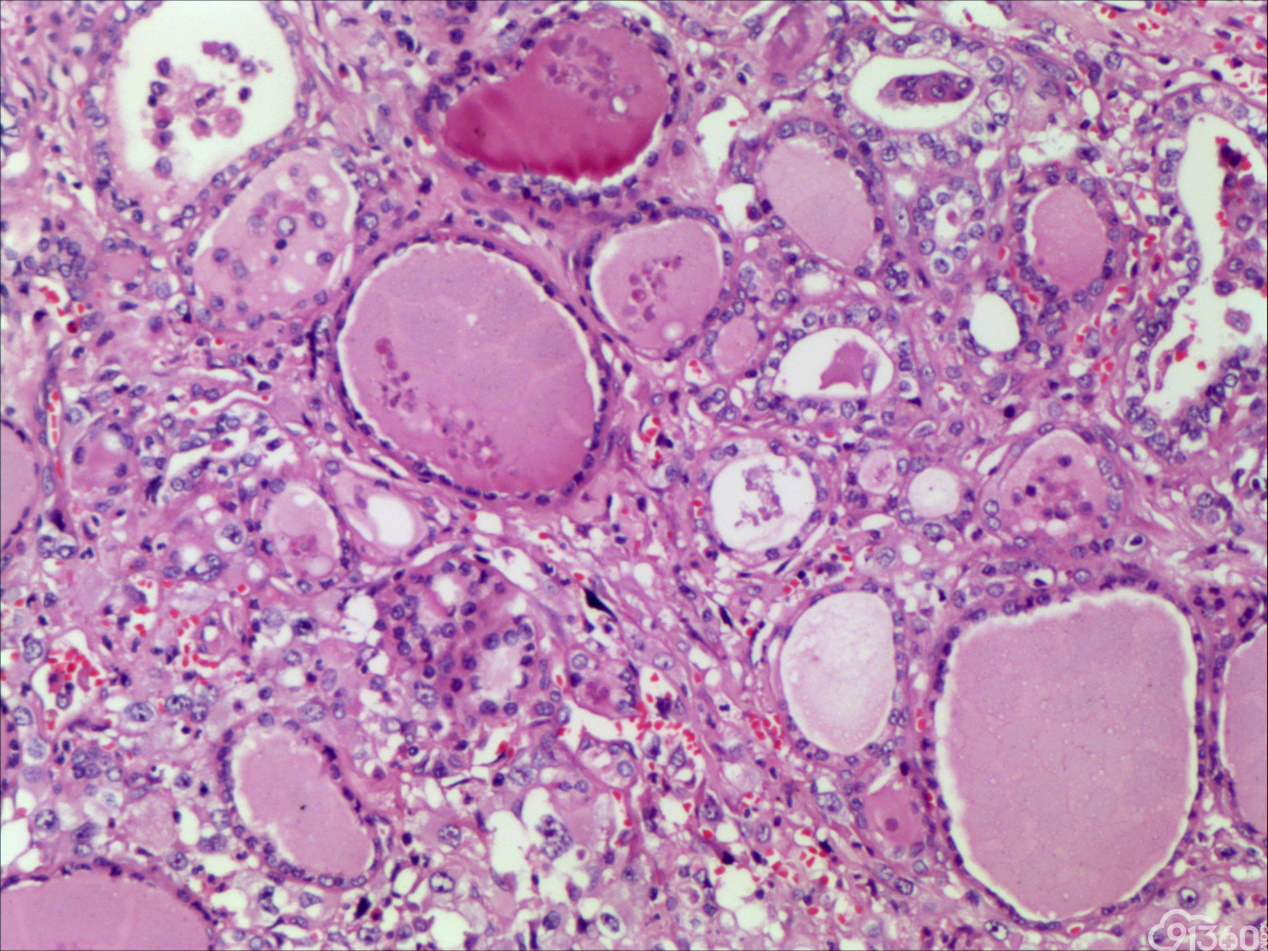 [/align][/align][/align]
[align=center][align=center][align=center] 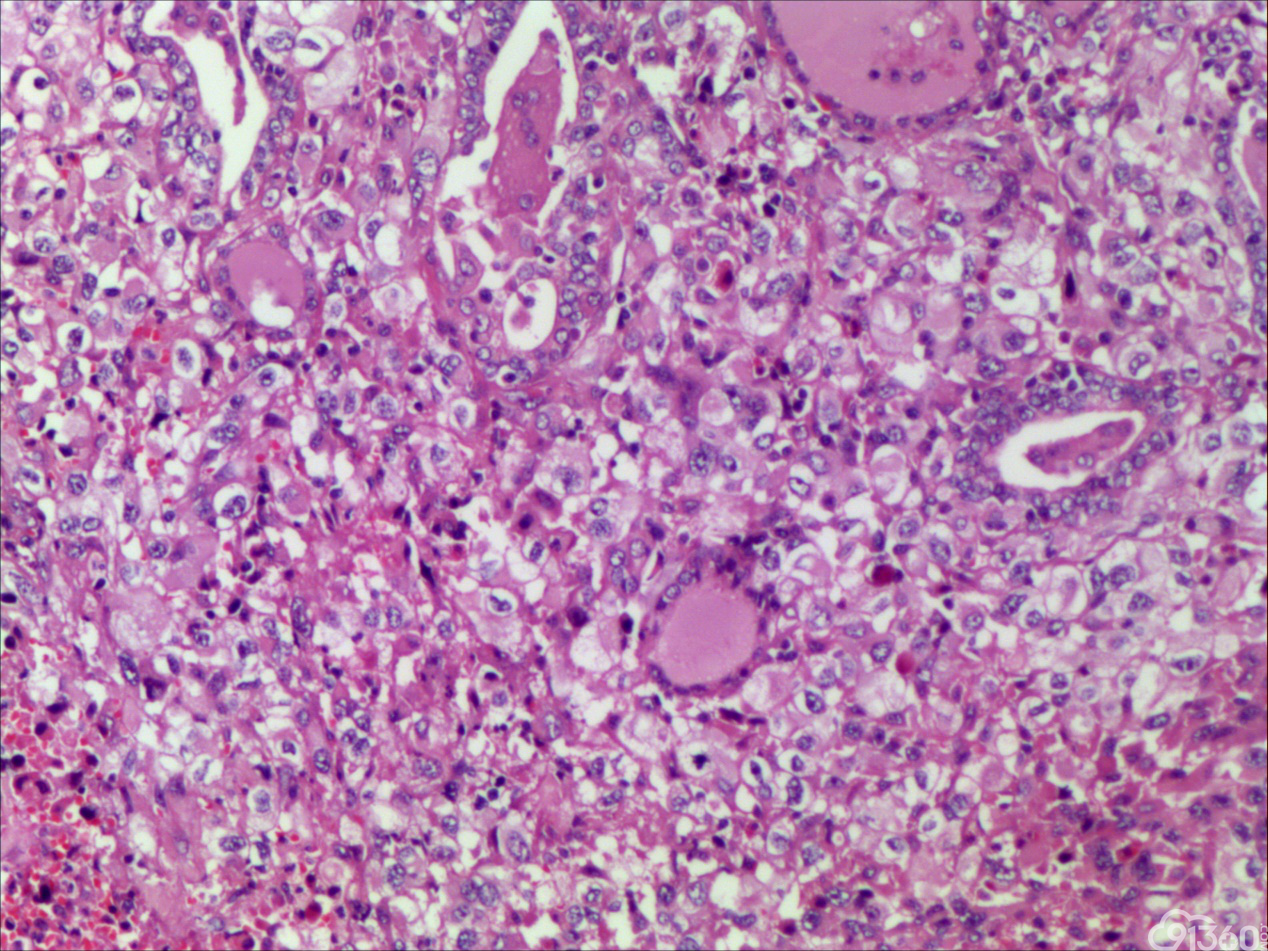 [/align][/align][/align]
[align=center][align=center][align=center] 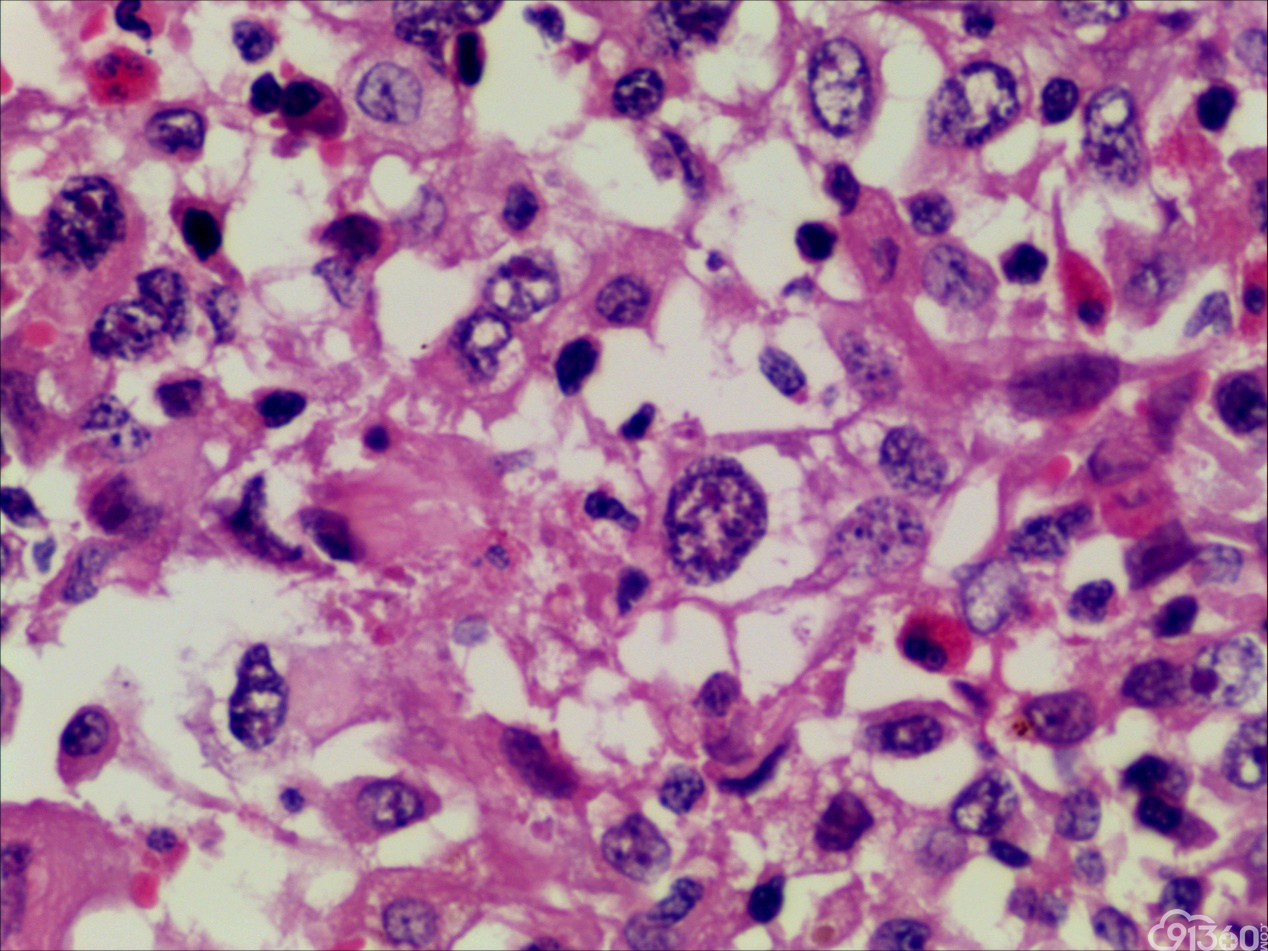 [/align][/align][/align]
[align=center][align=center][align=center] 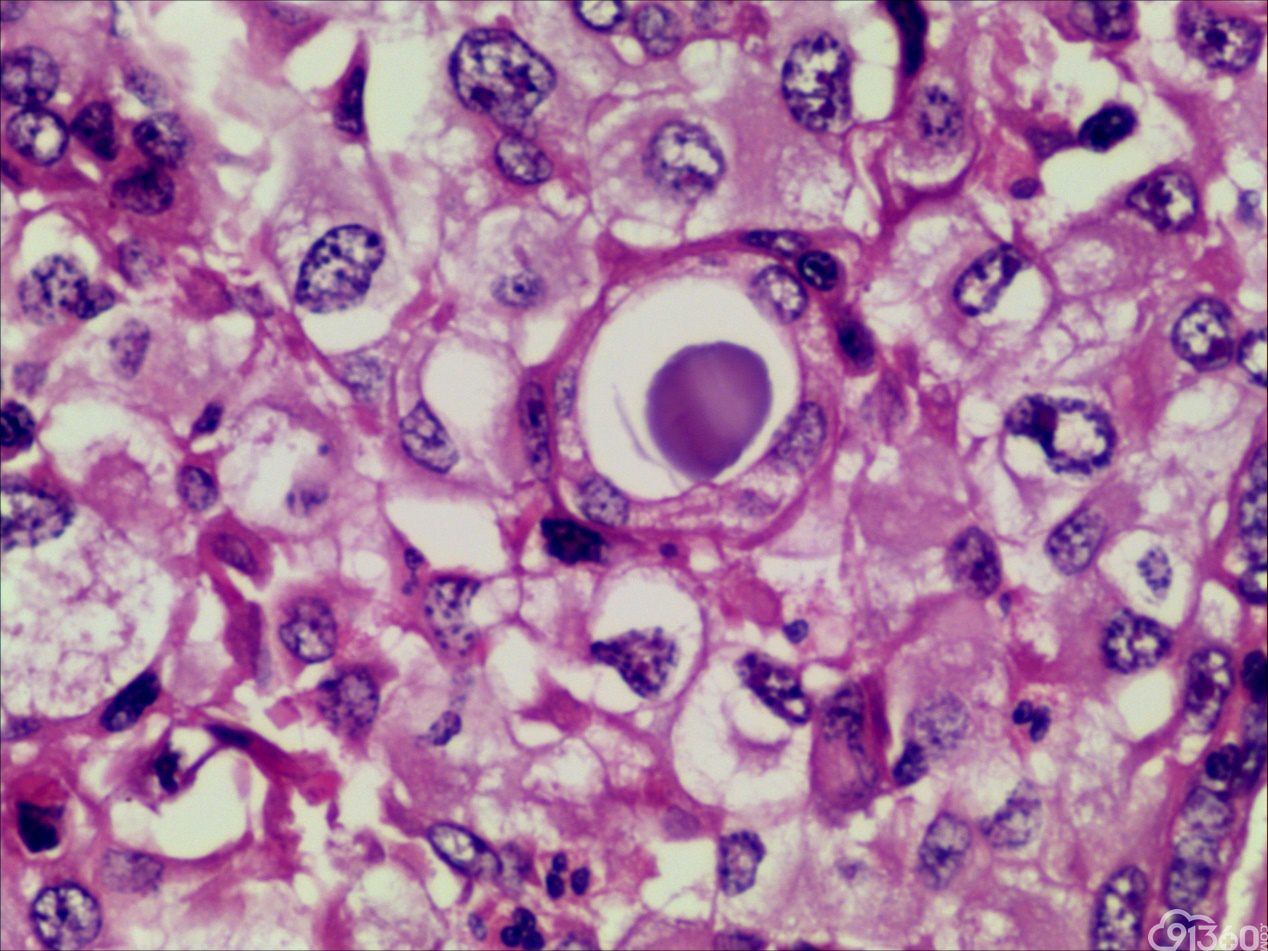 [/align][/align][/align]
[align=center][align=center][align=center] 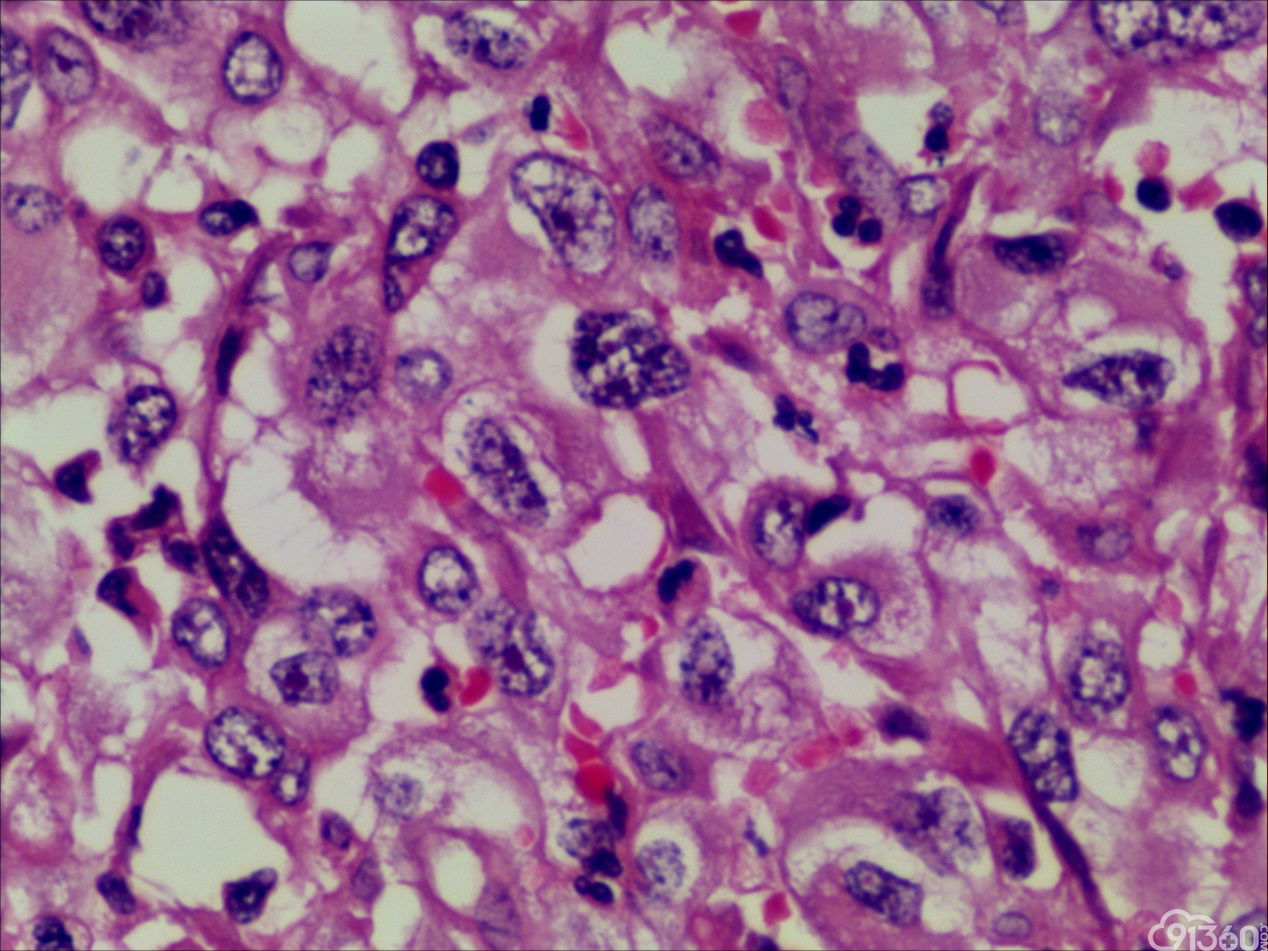 [/align][/align][/align] 免疫组化图:
[align=center][align=center][align=center]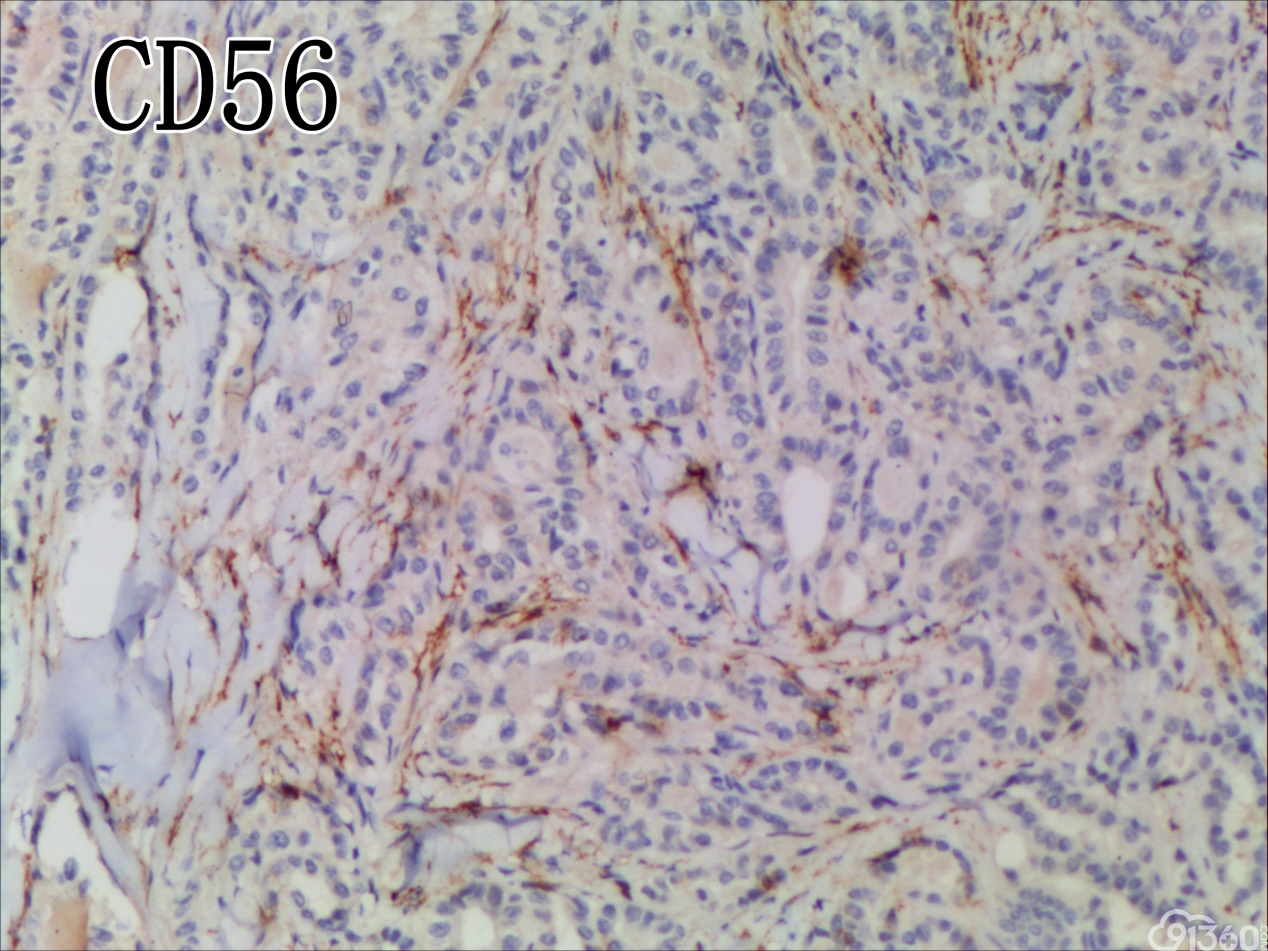 [/align][/align][/align] [/align][/align][/align]
[align=center][align=center][align=center]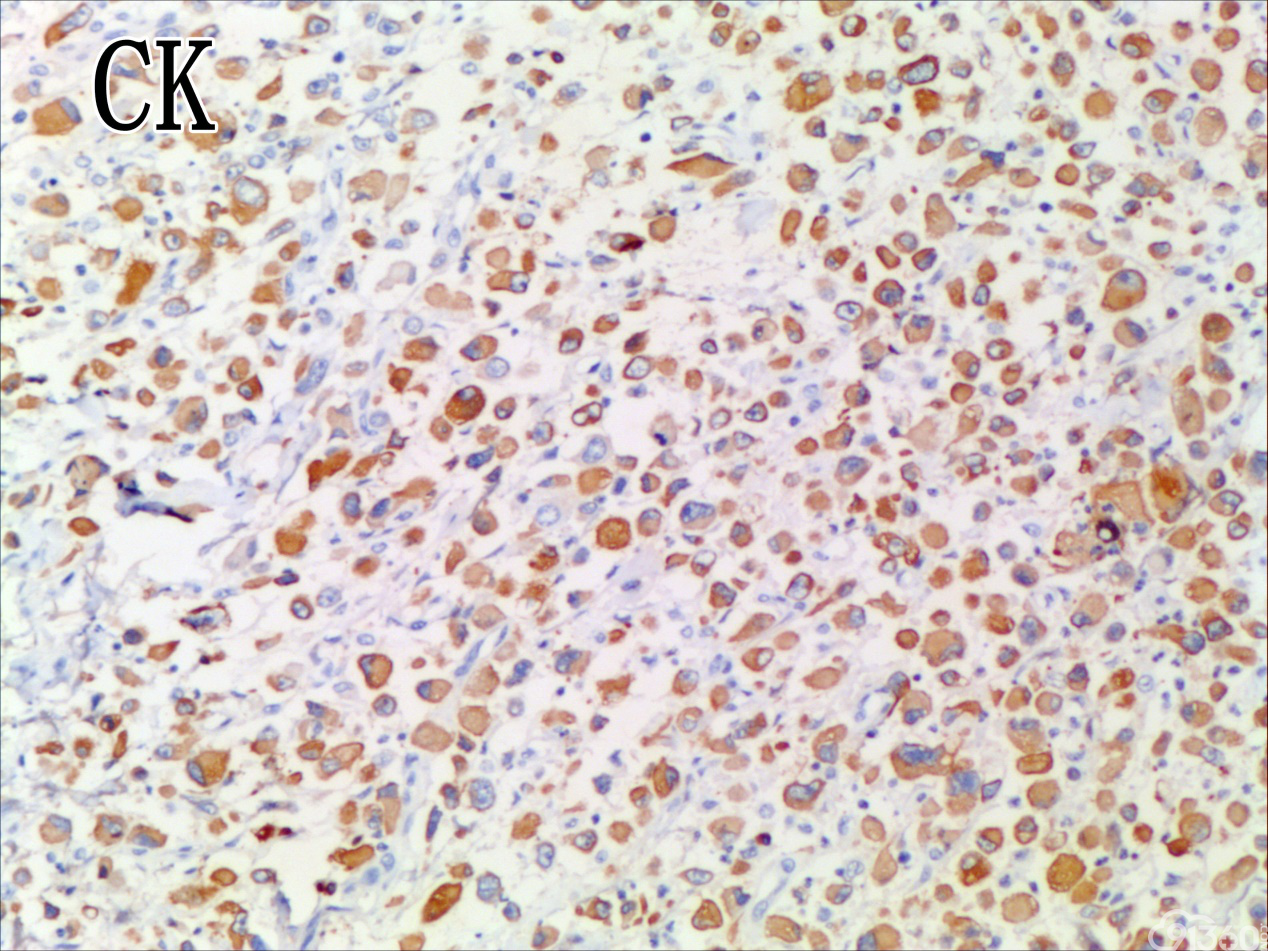 [/align][/align][/align] [/align][/align][/align]
[align=center][align=center][align=center]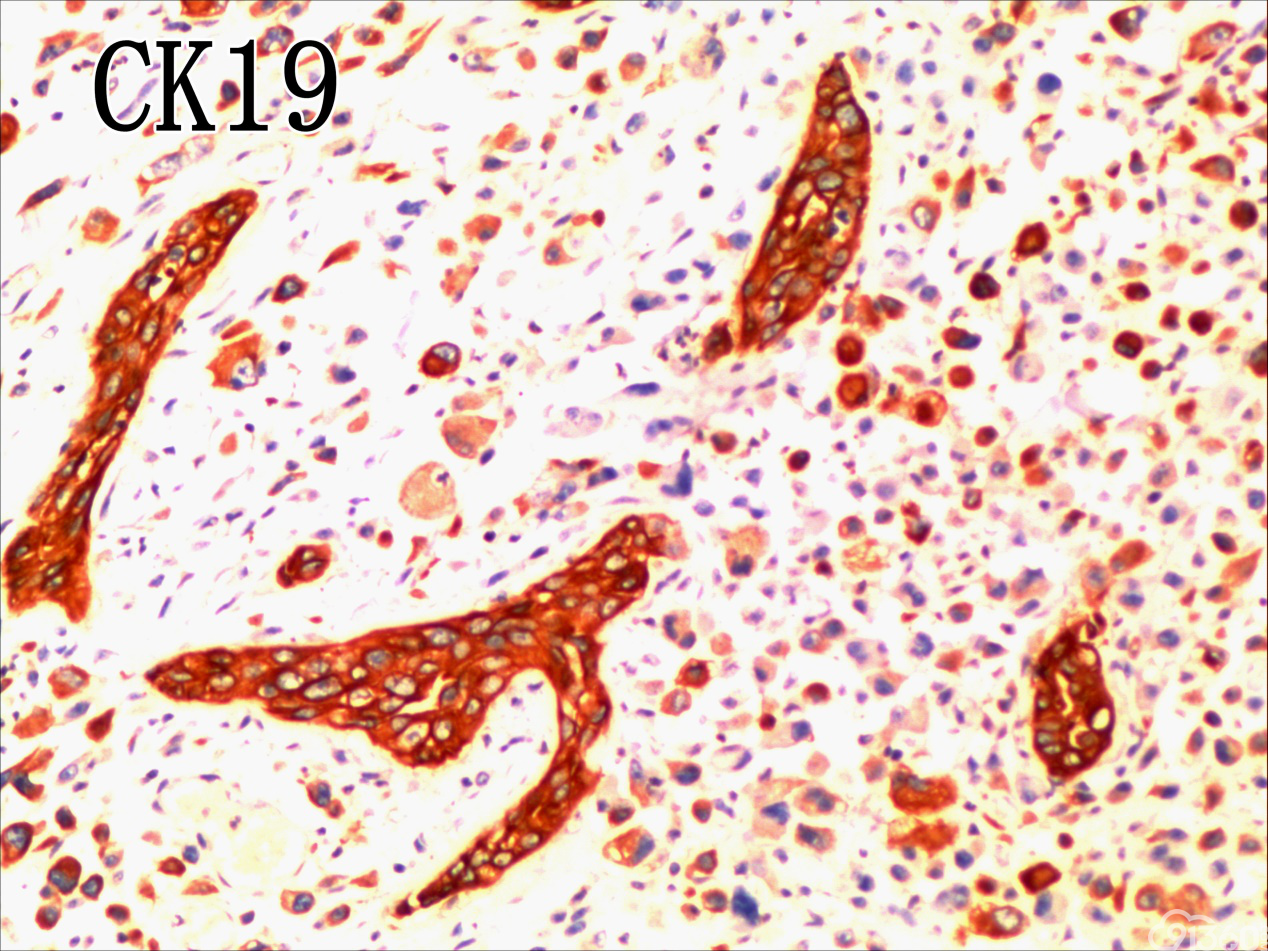 [/align][/align][/align] [/align][/align][/align]
[align=center][align=center][align=center]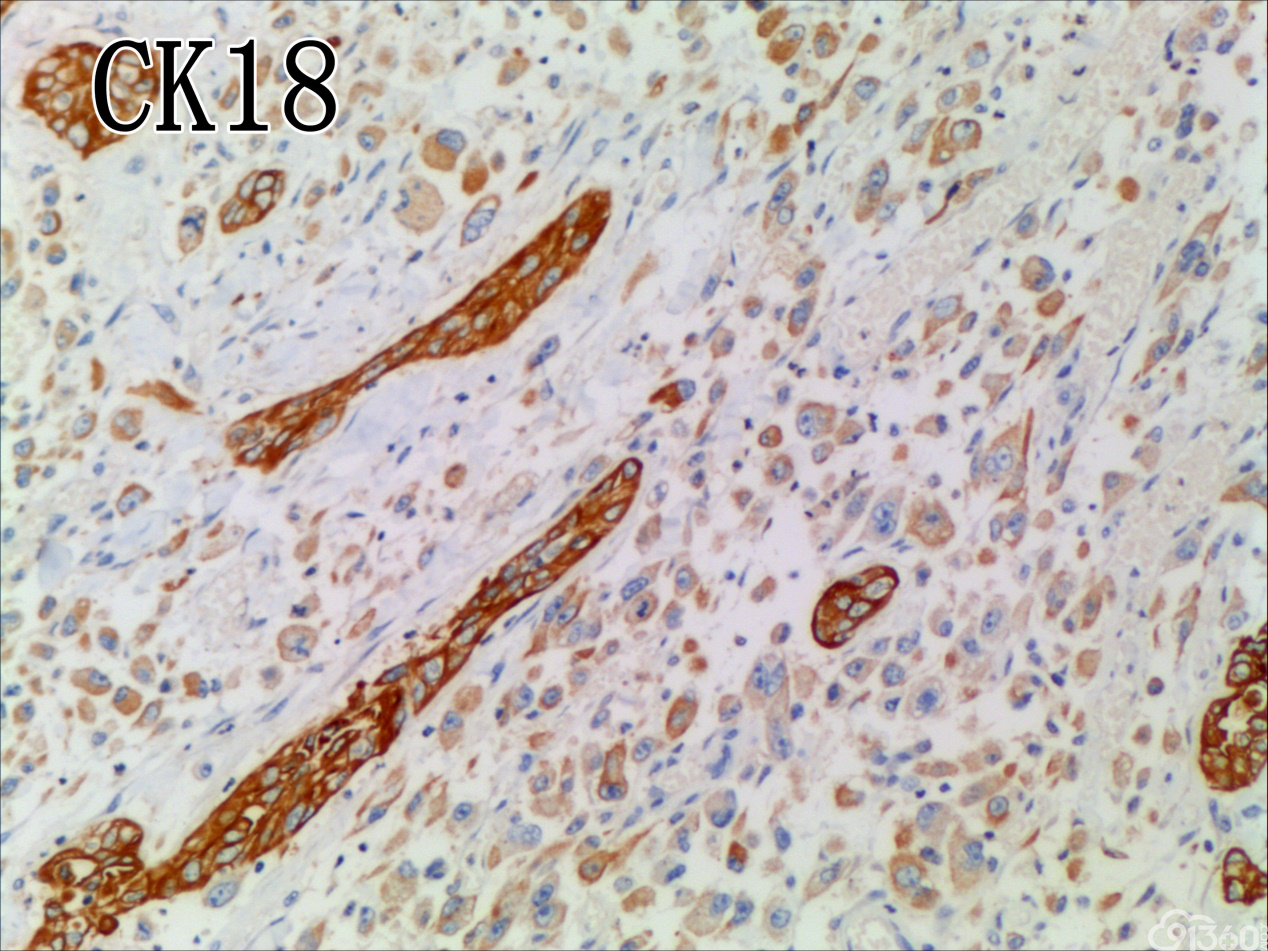 [/align][/align][/align] [/align][/align][/align]
[align=center][align=center][align=center]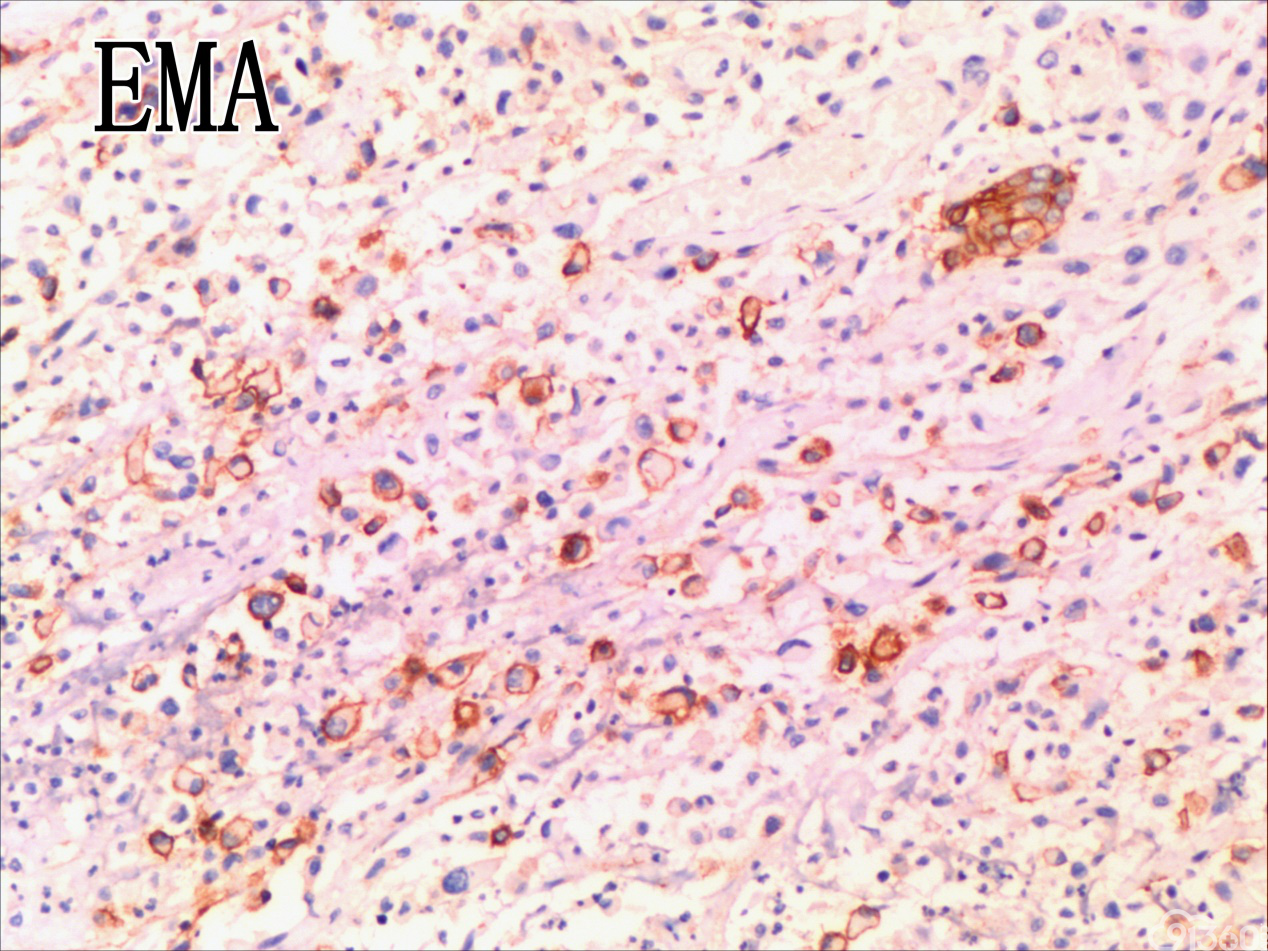 [/align][/align][/align] [/align][/align][/align]
[align=center][align=center][align=center]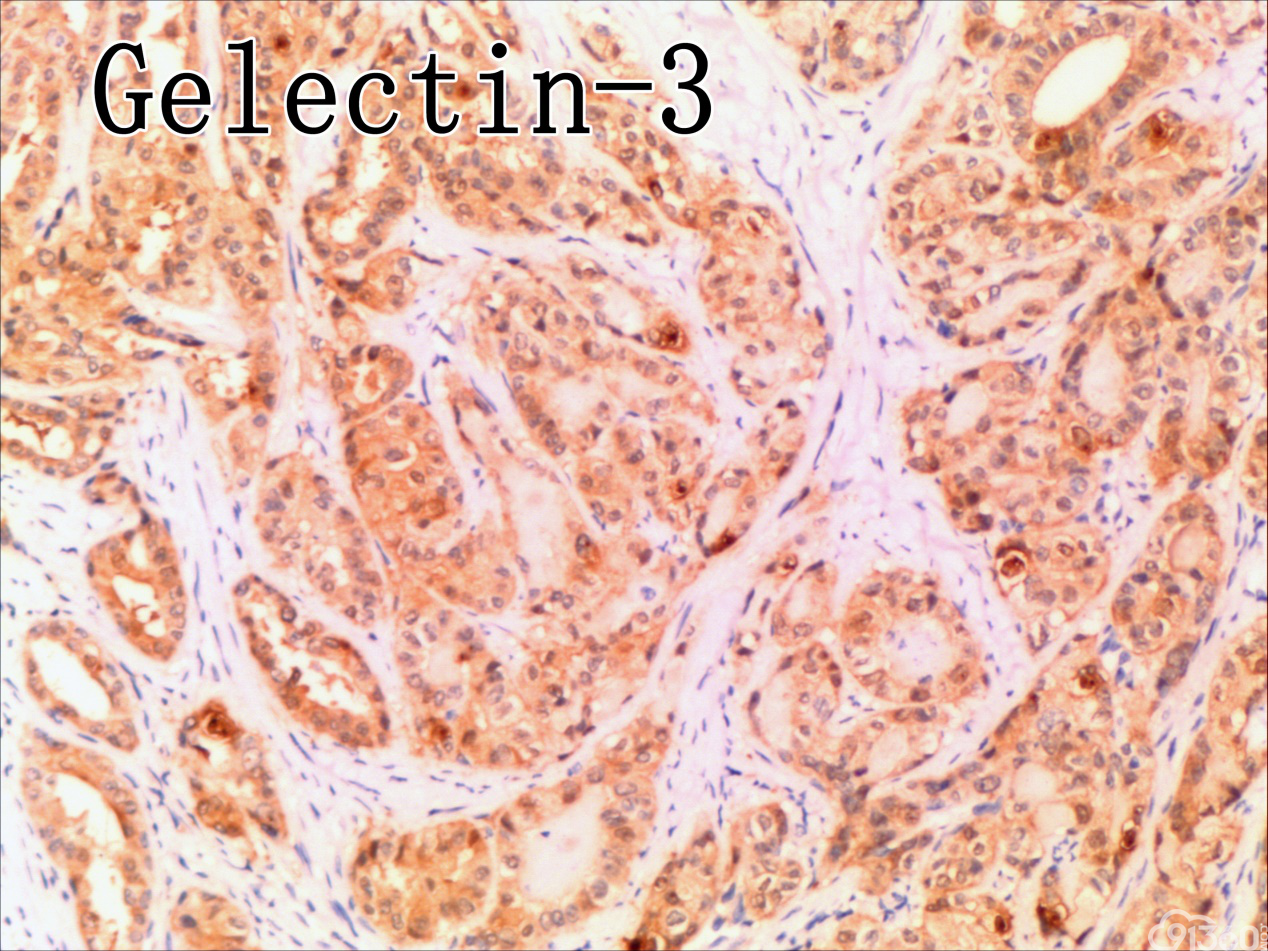 [/align][/align][/align] [/align][/align][/align]
[align=center][align=center][align=center]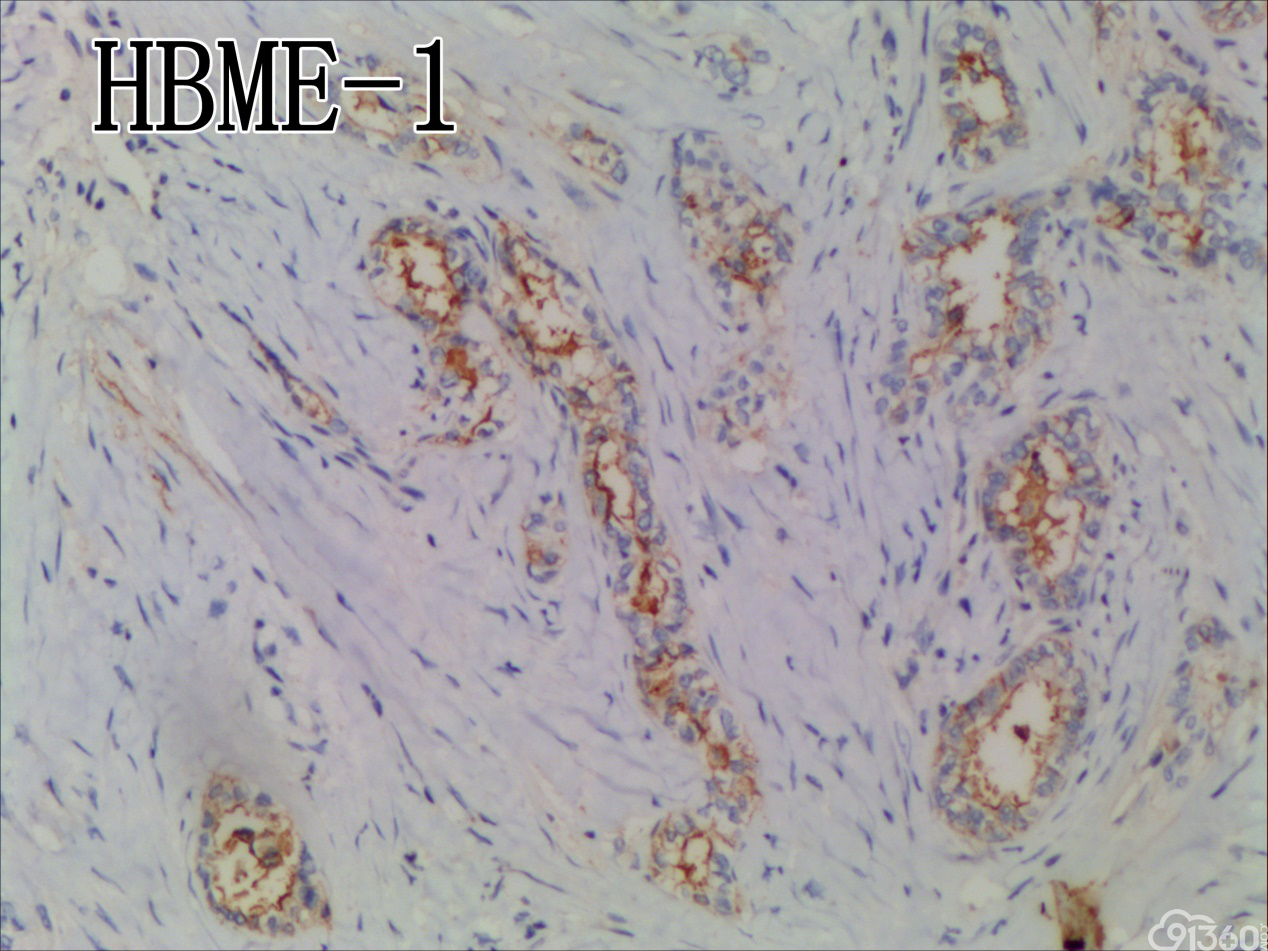 [/align][/align][/align] [/align][/align][/align]
[align=center][align=center][align=center]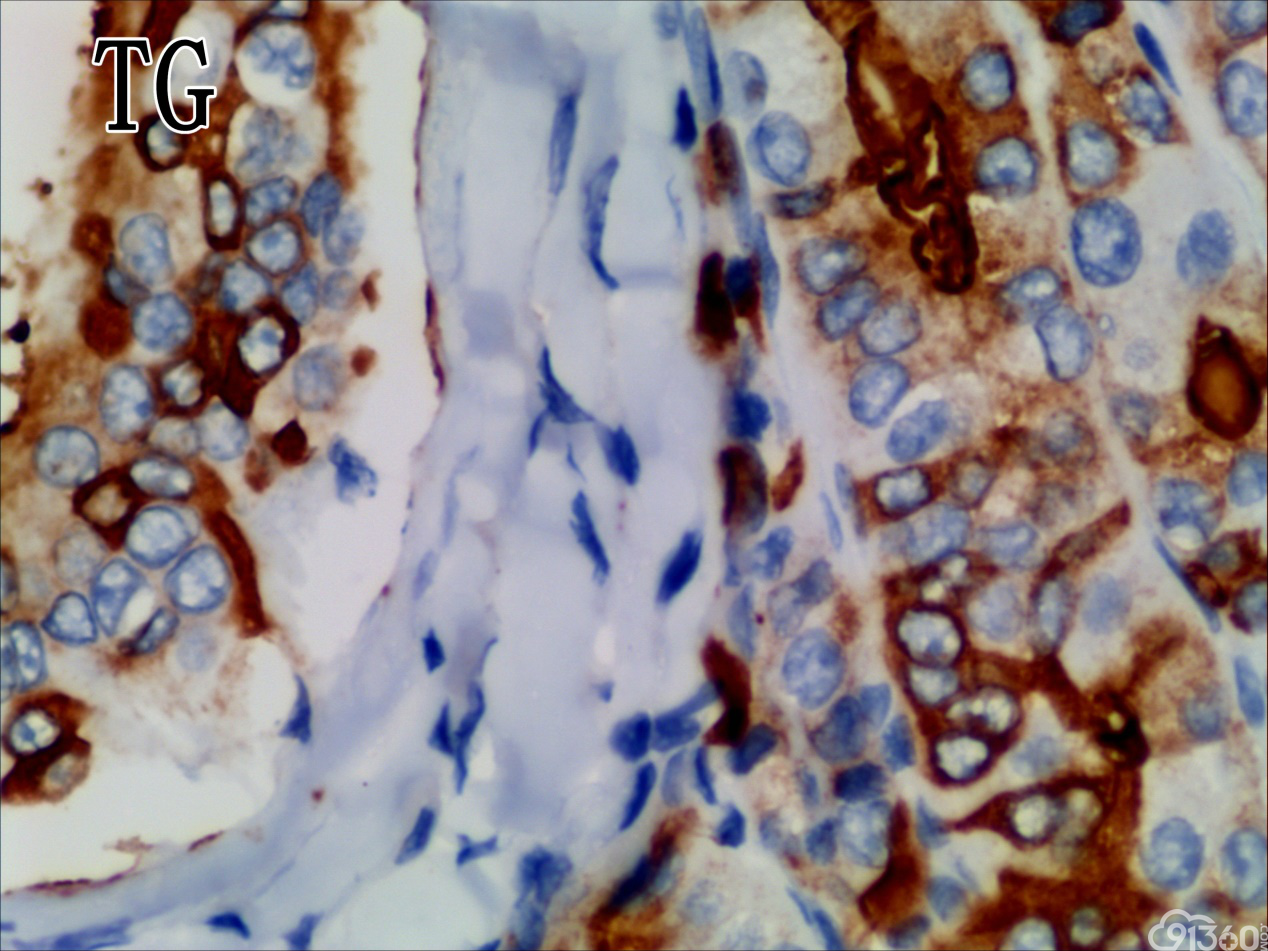 [/align][/align][/align] [/align][/align][/align]
[align=center][align=center][align=center]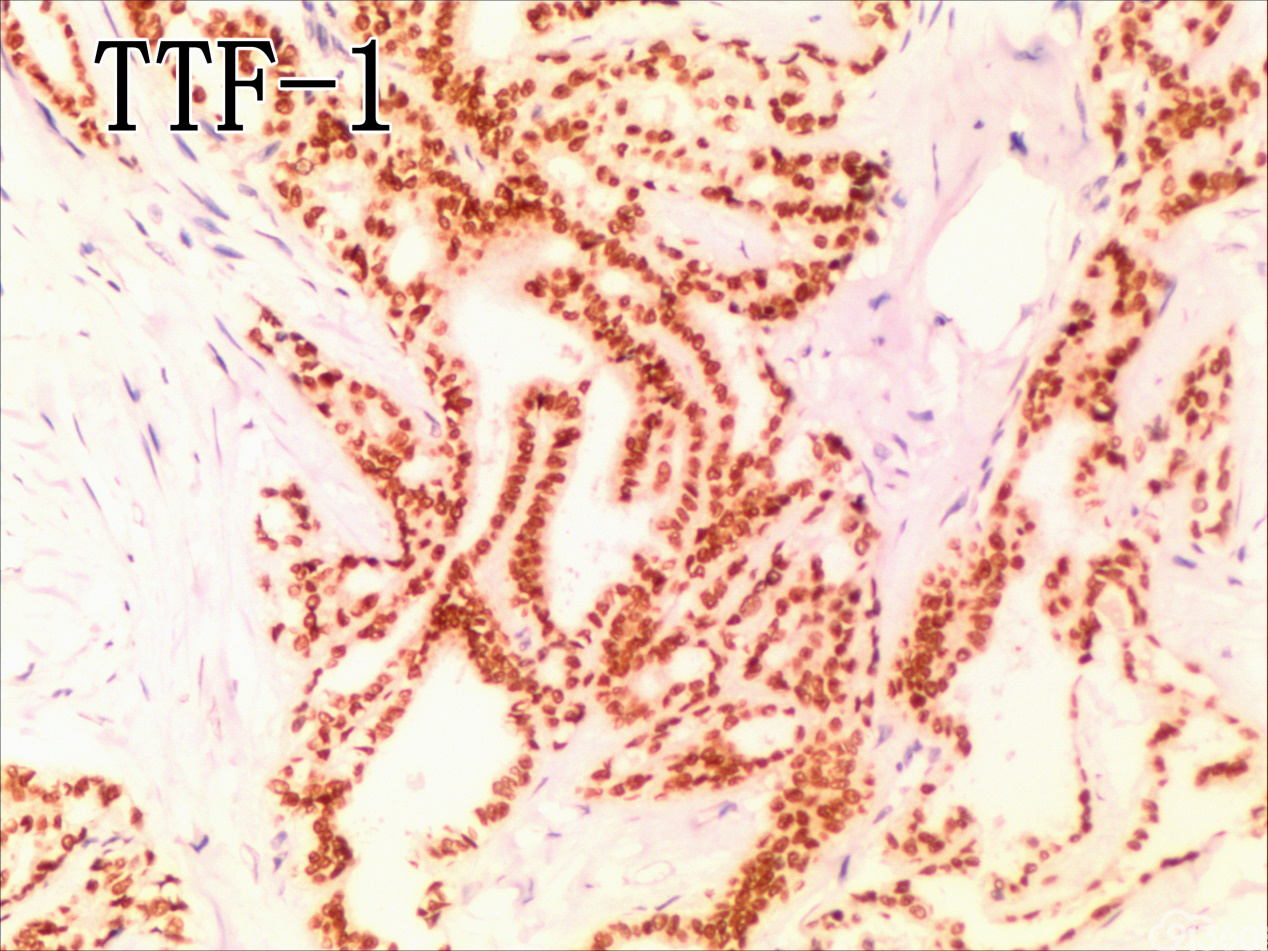 [/align][/align][/align] [/align][/align][/align]
[align=center][align=center][align=center]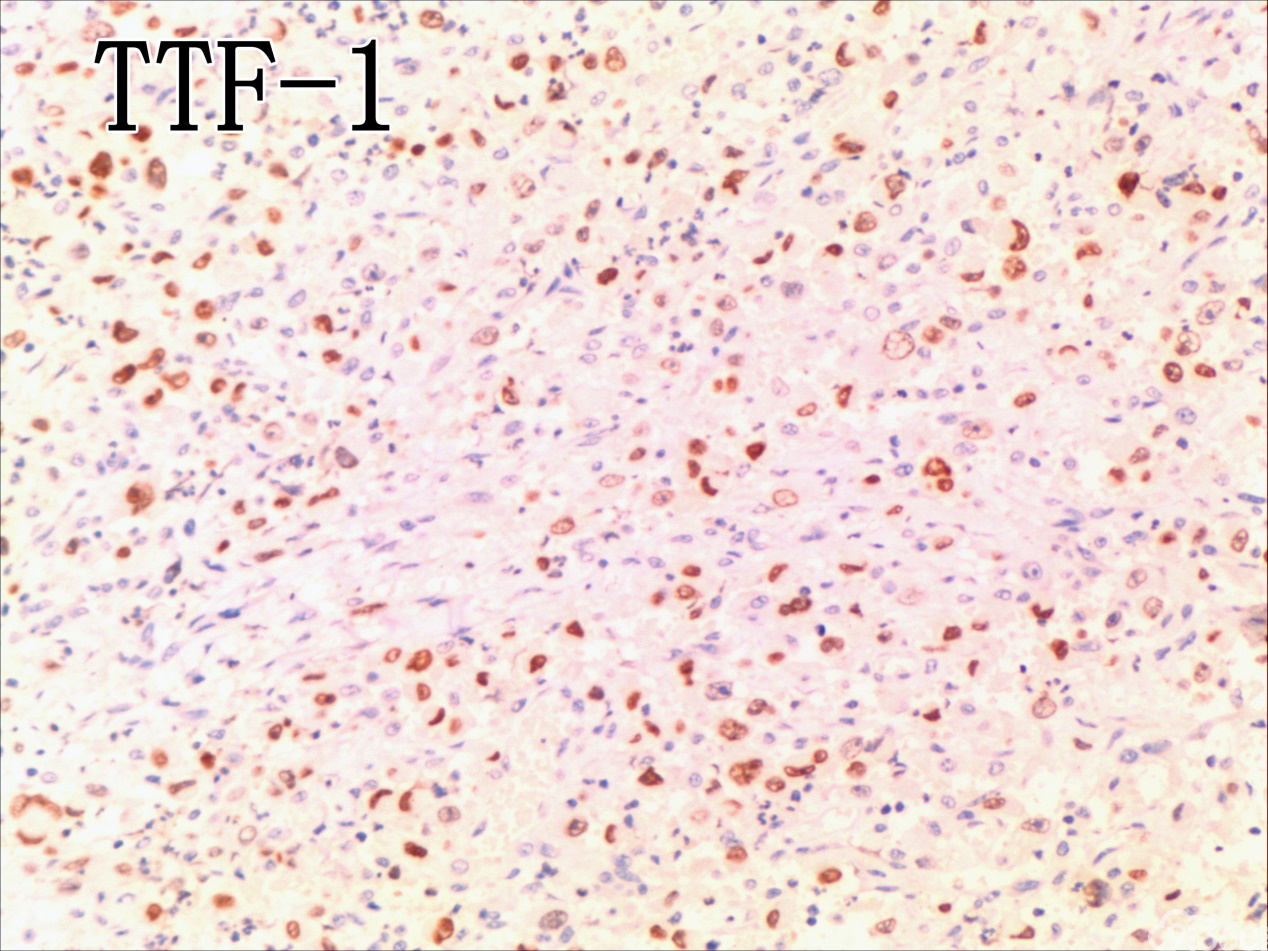 [/align][/align][/align] [/align][/align][/align]
[align=center][align=center][align=center]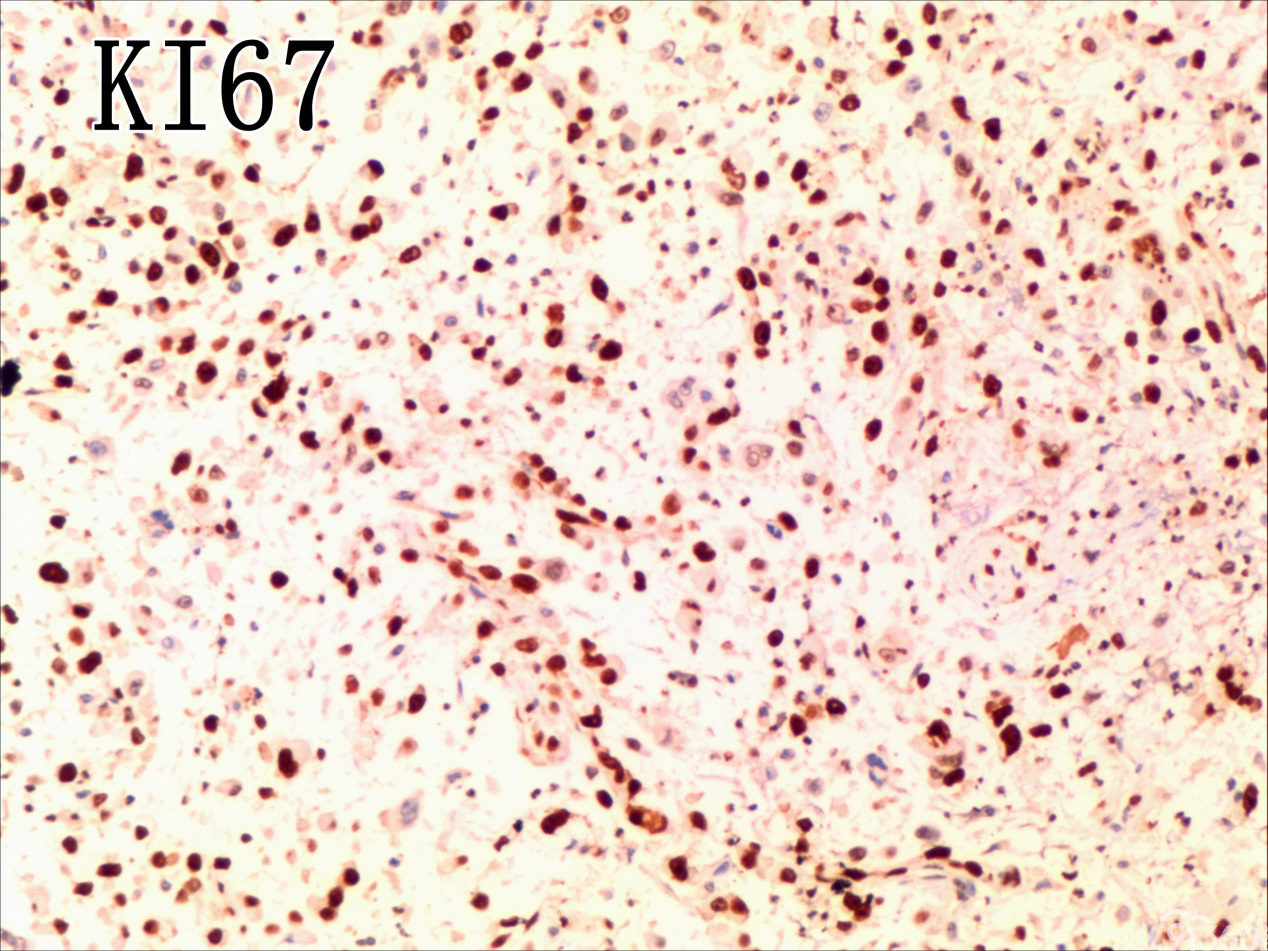 [/align][/align][/align] [/align][/align][/align]
免疫组化结果:Vimentin( )、TTF-1( )、CKpan( )、CK8/18( )、CK19( )、TG(部分细胞强阳性)、HBME-1(部分细胞阳性)、Gelectin-3(部分细胞阳性)、Ki-67( ,60%)、TPO(-)、Calcitonin(-)、PTH(-)、CD56(部分细胞弱阳性)、Syn(-)、CgA(-)、EMA(部分细胞阳性)。
诊断:甲状腺间变癌(ATC),侵犯神经。
讨论:
分化型甲状腺乳头状癌同时具备两种同源癌的成分,即甲状腺分化型癌和由其转化而来的甲状腺未分化或低分化癌。本例甲状腺乳头状癌的癌细胞和未分化癌细胞的免疫组化表达相一致也证实了二者同源。去分化代表着一个由高分化向低分化或未分化转化的过程,未分化成分的比例越大,恶性度越高。本例未分化癌成分占大部分,所以恶性度和预后应该与甲状腺未分化癌基本一致。本例乳头状癌成分较少,约25%左右。部分病例HE染色很难确定上皮或是间叶成分。免疫组化在区别间叶与上皮细胞方面更具客观性和说服力,但甲状腺滤泡上皮也可vimentin阳性,仅凭此不能区分甲状腺未分化癌和问叶组织肿瘤。未分化成分表达CK和Vimentin,而且CKl9和Galectin-3也阳性表达,因此需要选择多种抗体组合运用才能发挥其作用。如果在部分病例没有发现明显的侵蚀神经的现象,很可能把所有梭形细胞当成增生的纤维组织及纤维母细胞,导致误诊,本例去分化成分主要为未分化癌成分,如果存在较多的纤维性成分时候需要引起重视。
甲状腺未分化癌(undifferentiated thyroid carcinoma,UTC)又称间变性癌(anaplastic thyroid carcinoma,ATC),是比较罕见的一种癌,为高度恶性上皮性肿瘤,占所有甲状腺癌不足5%。UTC也是全身最致命性肿瘤之一,死亡率超过90%,中位生存期仅7个月左右。UTC常见于老年人,中位年龄为66岁,女性多于男性,通常表现为快速增大的甲状腺结节。UTC全部或部分由未分化细胞构成,可直接发生于甲状腺滤泡,亦可发生于分化好的甲状腺癌,此类细胞仅能通过免疫表型或超微结构辨识其上皮源性。由于在形态学上UTC表现形式多样,与其他甲状腺原发性肿瘤可有部分形态重叠,甚至免疫与遗传学特点亦有重叠,因此其鉴别诊断非常困难。UTC组织学特点取决于梭形细胞、鳞状或上皮样细胞、巨细胞三种主要细胞成分的构成,表现为以梭形主的肉瘤样形态,以上皮样细胞为主的癌样形态,或两者混合,而此例则表现为癌形态为主。肿瘤内常见显著的炎性背景,尤其是中性粒细胞及淋巴细胞,类似富含炎性细胞的未分化肉瘤。骨、软骨、横纹肌以及对应肿瘤的结构都可以出现异源性成分,尤其表现为横纹肌、破骨样多核巨细胞分化时,代表了一种少见形态变异亚型。在以上皮样细胞为主时,组织形态相对均一,细胞呈多边形,胞质丰富,核圆,细胞排列成假腺样或实性巢片状,混杂有多少不等的纤维性间质成分,在20%的病例中可见到鳞样分化,但往往与其他梭形、巨细胞成分混合。当上皮样细胞分化较差、巢片状分布、伴大量淋巴及浆细胞浸润时。在肿瘤取材充分的情况下,往往三种形态的细胞成分都能发现,混合存在,尤以一或两种成分为主[1]。
免疫表型与分子遗传学特点:
UTC的免疫表型比较复杂,表现多样化,上皮源性标记角蛋白(CK系列)阳性率为50-100%不等,单独的CK染色结果常表现不一致,一般联合几种CK套餐检测检出率可提高。上皮膜抗原(EMA)主要表达于上皮样分化的细胞中(40%左右),而间叶标志Vimentin在所有梭形细胞中都有表达。肿瘤细胞不表达甲状腺球蛋白(Tg)、促甲状腺激素(TSH)、降钙素及甲状腺转录因子(TTF-1)等组织特异性标志,却一致性强表达TP53。近年来研究发现,一种转录因子配对盒基因(PAX-8)在78%的UTC中有表达,而在头颈部的其他鳞癌中不表达。UTC的分子遗传学改变也是具有多样性的,但在众多差异中又有其独特性:①体细胞基因突变:主要发生于细胞信号转导通路的几个节点。在6%~50%UTC的病例中有RAS基因突变,在乳头状癌常见RET/PTC基因重排,而在UTC中几乎未发现,类似的Braf基因突变发生率在1/4左右,明显低于乳头状癌的50%。TERT启动子的突变发生率为33%~50%,尤其在Braf或RAS突变患者,可能在疾病后期进展中发挥作用。在25%~60%的UTC存在CTNNB1(β-catenin)突变,影响细胞黏附与上皮间质转化。除了促癌基因激活,抑癌基因失活也起有重要作用,超过50%的UTC有p53基因失活性突变,而PTEN为4%~16%。②染色体异常:研究发现UTC基因组的不稳定性与DNA拷贝量的变化呈异质性,尚无特异性结果,且染色体基因组的异常与UTC的生物学特点及结局不完全相关。③表观遗传学改变:主要涉及DNA甲基化与组蛋白修饰、沉默基因表达等,在肿瘤的去分化与增殖异质性上发挥重要作用,仅陆续发现与分化相关的基因SLC5A5及NKX2-1甲基化。另外,在甲状腺癌中,组蛋白H3的乙酰化呈高水平,利用组蛋白去乙酰化抑制剂可促进甲状腺癌细胞再分化,改善其对化疗药物的敏感性,说明UTC存在明确的潜在治疗预期的表观遗传学改变。
鉴别诊断:
1.孤立性纤维瘤:肿块中等大小,界限较清,纤维母细胞样,肿瘤细胞多围绕薄壁分支血管呈外皮瘤样排列,杂乱的胶原化,常CD34 ,STAT6 ,CK-,BCL2 ,CD99 。
2.Riedel甲状腺炎:临床大多表现为甲状腺功能低下,血中Tg抗体阳性,腺叶弥漫病变。镜下表现为炎性纤维性背景,细胞一般无异形,无上皮成分,累及周围组织。组化表现为,CK-,TTF1-,Tg-。
3.透明变梁状肿瘤:临床表现为孤立结节,生长缓慢,良性病程。镜下为梭形改变的滤泡上皮,排列成巢或梁状,纤细的透明变性间质。免疫组化:Tg ,TTF1 ,CK19 /-。
4.乳头状癌梭形细胞型:临床与乳头状癌类似。镜下:梭形细胞排列成束状,核保留乳头状癌特点。组化:CK ,SMA-,TPO-,Syn-,TTF1 ,Tg ,Calcitonin-。
5.髓样癌梭形细胞型:临床为孤立结节,腺叶上2/3,血钙异常,类癌综合征。镜下:巢片状、梁状排列,有致密胶原分隔,内淀粉样物质沉积。组化表现:CK ,Tg-,TTF1 ,SYN ,Calcitonin 。
6.恶性周围神经鞘膜瘤:与神经关系密切,孤立肿块,界清。镜下:密集与疏松区交替分布,疏松区有黏液性背景,核分裂及坏死多见。组化,S100 /-,SOX10 /-,Vimentin ,其他(-)。
7.伴胸腺成分的梭形上皮性肿瘤(settle):儿童及青年,无痛性肿块。肿瘤呈双相分化(梭形细胞为主 腺管样结构),两者有融合CK 、CD5-,Tg-,SMA梭形细胞 ,S100-,CEA-,Syn-。
8.鳞癌:原发或转移性,由肿瘤性鳞状上皮构成(角化珠、细胞间桥)CK ,P63 ,Tg-,PAX8-。
9.伴嗜酸粒细胞增多的硬化性黏液表皮样癌:一般病程缓慢,桥本性甲状腺炎病史,由表皮、黏液上皮细胞及嗜酸粒细胞构成,纤维化背景,CK ,TTF1 /-,Tg-。
10.呈胸腺样分化的癌(castle):多为中年,无痛性肿块,鳞样及梭形细胞分隔呈小叶状,类似胸腺癌,伴淋巴细胞浸润CK ,CD5 ,Tg。
总结
甲状腺恶性肿瘤的诊断存在较大的争议,由于乳头状癌和滤泡性肿瘤之间存在相互的形态学交叉很容易导致诊断错误。而未分化甲状腺癌更是少见,且结构存在很大的差异,需要结合免疫组化及分子等手段。总而言之,对于甲状腺肿瘤的诊断需要在HE形态的基础之上再结合免疫组化结果及分子检测结果,才能做到心中有数。
参考文献
[1]唐峰, 杜尊国。 浅谈甲状腺未分化癌的病理诊断[J]. 上海医药, 2016,37(6):7-10.
|